
【题目】可逆反应![]()
![]() 在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
| 1.向甲烧杯中加入 2.向乙烧杯中投入一定量的 |
(1)甲烧杯中![]() 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡![]() 向______________(填“正反应”或“逆反应”)方向移动,所以
向______________(填“正反应”或“逆反应”)方向移动,所以![]() 晶体溶于水是__________________(填“放热”或“吸热”)过程。
晶体溶于水是__________________(填“放热”或“吸热”)过程。
(2)根据乙烧杯中的现象,补全![]() 与
与![]() 反应过程的能量变化示意图_____。
反应过程的能量变化示意图_____。

科目:高中化学 来源: 题型:
【题目】已知:Ksp(AgCl)=1×10-10,Ksp(AgI)=1×10-16,Ksp(Ag2CrO4)=8.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A. AgCl>AgI>Ag2CrO4 B. AgCl>Ag2CrO4>AgI
C. Ag2CrO4>AgCl>AgI D. Ag2CrO4>AgI>AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解槽装置如图所示,用Cu-Si合金作硅源,在950℃利用三层液熔盐进行电解精炼,有关说法正确的是

A.电子由液态Cu-Si合金流出,流入液态铝电极
B.液态铝电极与正极相连,作为电解池的阳极
C.在该液相熔体中Cu优先于Si被氧化,Si4+优先于Cu2+被还原
D.三层液熔盐的作用是使电子能够在三层间自由流动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)做电极材料。对LiFePO4废旧电极(含杂质Al、石墨粉)回收并获得高纯Li2CO3的工业流程如图:
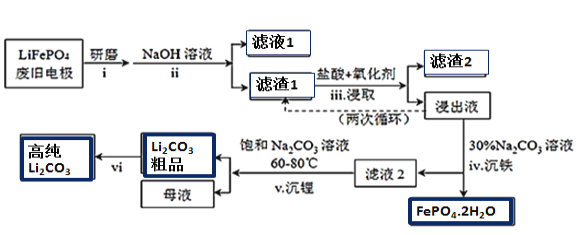
资料:碳酸锂在水中溶解度随温度变化如下:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)过程i研磨粉碎的目的是__________________。
(2)过程ii加入足量NaOH溶液的作用(用化学反应方程式表示)_________________。
(3)如过程iii采用NaClO3作为氧化剂,则过程中会反应会发生副反应生成黄绿色气体,
①该副反应对应的离子方程式为_______________________________________________________;
从环保角度分析,选择___________(填字母)作为该过程的氧化剂会更好。
a.H2O2 b.浓硫酸 c.浓HNO3
②过程iii得到的浸出液循环两次的目的是________________________________________________。
(4)浸出液中存在大量H2PO4﹣和HPO42-,已知:![]() ,结合平衡移动原理,解释过程iv得到磷酸铁晶体的原因______________________________________。
,结合平衡移动原理,解释过程iv得到磷酸铁晶体的原因______________________________________。
(5)简述过程vi的操作______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的用途利用了其还原性的是( )
A. 用葡萄糖制镜子或保温瓶胆
B. 用硫粉覆盖洒落在桌上的Hg
C. 用![]() 溶液制备木材防火剂
溶液制备木材防火剂
D. 用![]() 作为高效水处理剂
作为高效水处理剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 在不同的溶剂中可形成不同的分散系:
在不同的溶剂中可形成不同的分散系:![]() 溶解在水中形成无色透明的分散系一;
溶解在水中形成无色透明的分散系一;![]() 溶解在乙醇中形成无色透明的分散系二。下列说法正确的是( )
溶解在乙醇中形成无色透明的分散系二。下列说法正确的是( )
A. 分散系二与雾、霾为同一种类型的分散系
B. 在两个分散系中,![]() 都是以
都是以![]() 和
和![]() 的形式存在
的形式存在
C. 分散系二中,分散质粒子的个数为![]() 个
个
D. 两个分散系都是电解质且性质较稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锰是化学工业中常用的氧化剂和催化剂。我国主要以贫菱锰矿(有效成分为![]() )为原料,通过热解法进行生产。
)为原料,通过热解法进行生产。
(1)碳酸锰热解制二氧化锰分两步进行:
i.![]()
ii. ![]()
①反应i的化学平衡常数表达式![]() ___________。
___________。
②焙烧![]() 制取
制取![]() 的热化学方程式是_________________。
的热化学方程式是_________________。
(2)焙烧(装置如图1)时持续通入空气,并不断抽气的目的是________________。
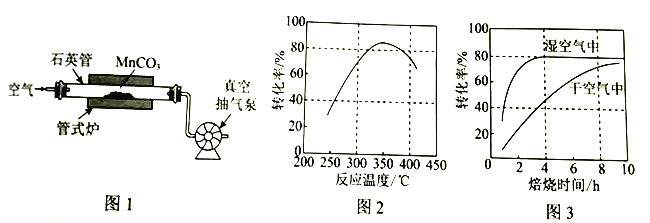
(3)在其他条件不变时,某科研团队对影响![]() 转化率的生产条件进行了研究,结果如图2、图3所示。
转化率的生产条件进行了研究,结果如图2、图3所示。
①图2是在常压(![]() )下的研究结果,请在图2中用虚线画出
)下的研究结果,请在图2中用虚线画出![]() 下
下![]() 转化率与反应温度的关系图______。
转化率与反应温度的关系图______。
②常压下,要提高![]() 的转化率,应选择的生产条件是____________焙烧
的转化率,应选择的生产条件是____________焙烧![]() 。
。
③图3中,焙烧![]() 时,
时,![]() 的转化率:干空气<湿空气,原因是______________。
的转化率:干空气<湿空气,原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体的健康有赖于体内各种元素的均衡摄入。
(1)正常人一天的食盐摄入量不超过 6g。
①除去 NaCl溶液中的SO42-,依次加入的溶液为(填溶质的化学式):过量______溶液、过量______溶液、适量稀盐酸。
②食用碘盐是食盐中加入 KIO3。下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。回答下列问题:
配料表 | 精制海盐、碘酸钾(KIO3) |
含碘量 | 20~40 mg/kg |
储藏方法 | 密封避光、防潮 |
食用方法 | 烹调时待食品熟后加入碘盐 |
食用碘盐中“碘”是指______(填“碘离子”或“碘元素”)。推测出碘酸钾(KIO3)化学性质:碘酸钾(KIO3)在高温时______(填“易分解”或“不易分解”)。一种测定含碘量的化学原理是:
(Ι)KIO3 + KI + H2SO4===K2SO4 + I2 + H2O(未配平),
(Ⅱ)I2 + 2Na2S2O3 = 2NaI + Na2S4O8。将反应 Ι 改写为离子方程式_____
(2)成人每天从食物中摄取 0.8 g Ca 元素、0.3 g Mg 元素。
①Ca 元素与 Mg 元素物质的量之比为______。
②墨鱼骨粉(主要成分是 CaCO3),可用作治疗胃酸过多,其原因是_________(用离子方程式回答)。
③从海水中可提取镁:除去混在 Mg(OH)2 中的 Ca(OH)2 的最佳方法是:加入过量的______(填“A”或“B”)(A. MgSO4 溶液 B. MgCl2 溶液),过滤,洗涤,低温烘干。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com