
【题目】标准状况下,2 mol O2和2 mol H2O相比较,下列叙述正确的是
A.分子数相等B.体积相等
C.质量相等D.原子数相等
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是( )
A.石灰石与盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
B.钠与水的反应:![]()
C.氢氧化铜溶于盐酸:Cu2++2OH-+2H+=Cu2++2H2O
D.氯气与水的反应: Cl2+H2O = 2H++Cl-+ClO—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应![]()
![]() 在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
| 1.向甲烧杯中加入 2.向乙烧杯中投入一定量的 |
(1)甲烧杯中![]() 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡![]() 向______________(填“正反应”或“逆反应”)方向移动,所以
向______________(填“正反应”或“逆反应”)方向移动,所以![]() 晶体溶于水是__________________(填“放热”或“吸热”)过程。
晶体溶于水是__________________(填“放热”或“吸热”)过程。
(2)根据乙烧杯中的现象,补全![]() 与
与![]() 反应过程的能量变化示意图_____。
反应过程的能量变化示意图_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是闪锌矿(主要成分是![]() ,含有少量
,含有少量![]() )制备
)制备![]() 的一种工艺流程:
的一种工艺流程:
![]()
资料:相关金属离子浓度为![]() 时形成氢氧化物沉淀的
时形成氢氧化物沉淀的![]() 范围如下:
范围如下:
金属离子 |
|
|
|
开始沉淀的 | 1.5 | 6.3 | 6.2 |
沉淀完全的 | 2.8 | 8.3 | 8.2 |
(1)闪锌矿在溶浸之前会将其粉碎,目的是______________。
(2)溶浸过程使用过量的![]() 溶液和
溶液和![]() 浸取矿粉,发生的主要反应是:
浸取矿粉,发生的主要反应是:
![]() 。下列判断正确的是____________(填字母序号)。
。下列判断正确的是____________(填字母序号)。
a.浸出液中含有![]() 等阳离子
等阳离子
b.加入硫酸,可以抑制![]() 水解
水解
c.若改用![]() 溶液进行浸取,将发生反应:
溶液进行浸取,将发生反应:![]()
(3)工业除铁过程需要控制沉淀速率,因此分为还原和氧化两步先后进行,如下图。还原过程将部分![]() 转化为
转化为![]() ,得到
,得到![]() 小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入
小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入![]() 。
。
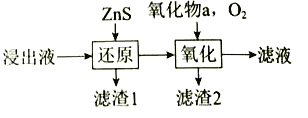
①a可以是______________,加入a的作用是_______________。
②除铁过程中可以控制溶液中![]() 的操作是_______________。
的操作是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
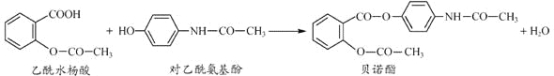
下列有关叙述正确的是( )
A. 贝诺酯分子中有三种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D. 贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种常见元素结构信息如下表,试根据信息回答有关问题:

(1)写出B原子的基态电子排布式__;
(2)用氢键表示式写出A的氢化物溶液中存在的氢键__(任写一种);A的氢化物分子结合一个H+形成阳离子后,其键角__(填写“变大”、“变小”、“不变”);
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为__,简要描述该配合物中化学键的成键情况__;
(4)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“”表示没有形成共价键的最外层电子,短线表示共价键.

在以上分子中,中心原子采用sp3杂化形成化学键是__(填写序号);在②的分子中有__个σ键和__个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 如图所示为二维平面晶体示意图,所表示的化学式为AX3的是________。

(2) 下图为一个金属铜的晶胞,请完成以下各题。

① 该晶胞“实际”拥有的铜原子数是________个。
② 该晶胞称为________(填序号)。
A.六方晶胞 B.体心立方晶胞
C.面心立方晶胞 D.简单立方晶胞
③此晶胞立方体的边长为a cm,Cu的相对原子质量为64 g·mol-1,金属铜的密度为ρ g·cm-3,则阿伏加德罗常数为________(用a、ρ表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、W是原子序数依次递增的五种短周期主族元素,它们所在周期数之和为11,其中Y元素最高与最低化合价的代数和为2,Y和Z的单质生成的化合物是一种传递神经信息的“信使分子”,R的原子半径是五种元素中最大的,Y和W是同族元素。下列说法错误的是( )
A. 简单离子的还原性:Y>Z
B. R的单质可能是金属或非金属
C. 由X、Z和W构成的酸一定是三元酸
D. 标准状况下,1molYZ与0.5mol![]() 混合后所得气体的体积一定小于22.4L
混合后所得气体的体积一定小于22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】In是第5周期ⅢA的元素;In2O3是一种透明的导电材料,可运用于触控屏、液晶显示器等高科技领域;利用水铟矿(主要成分In(OH)3),制备In2O3的工艺流程如下:
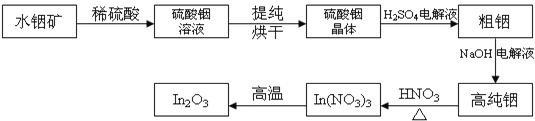
(1)写出水铟矿被硫酸酸溶的离子方程式:_____________________________。
(2)从硫酸铟溶液中制备硫酸铟晶体的实验步骤:___、___、过滤、洗涤和干燥。
(3)提纯粗铟的方法和铜的精炼原理相似,则粗铟为___(填“阴极”、“阳极”),写出阴极的电极反应式___________________________________。
(4)完成下列化学方程式:___In(NO3)3![]() ___In2O3+___↑+___↑。
___In2O3+___↑+___↑。
(5)高纯铟和浓硝酸反应过程中产生的NO2气体可以被Na2O2直接吸收,则标准状况下672mLNO2可以被___gNa2O2吸收。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com