
 2C(g)��4D(g)����H<0�ﵽƽ�⣨��ʱ��V(��)=1.21V L����ش�
2C(g)��4D(g)����H<0�ﵽƽ�⣨��ʱ��V(��)=1.21V L����ش�
 2C(g)��4D(g)
2C(g)��4D(g)


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
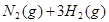
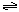
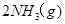
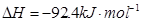 ����
����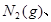 3mol
3mol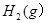 ����һ�ݻ�Ϊ2L���ܱ������У���500���½��з�Ӧ��10min
����һ�ݻ�Ϊ2L���ܱ������У���500���½��з�Ӧ��10min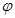 ������˵������ȷ���ǣ� ��
������˵������ȷ���ǣ� ��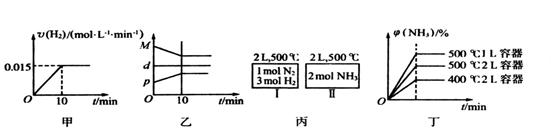
| A�����ﵽƽ��ʱ�������ϵ�ų�9.24kJ��������H2��Ӧ���ʱ仯������ͼ����ʾ |
| B����Ӧ�����У��������ƽ����Է�������ΪM����������ܶ�Ϊd���������ѹǿΪp�����߹�ϵ��ͼ�� |
C����ͼ����ʾ������I��II�ﵽƽ��ʱ��NH3���������Ϊ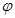 ��������I�ų�����������II��������֮��Ϊ92.4kJ ��������I�ų�����������II��������֮��Ϊ92.4kJ |
| D������ʼ��������Ϊ1 mol N2��3 mol H2���ڲ�ͬ�����´ﵽƽ��ʱ��NH3����������仯��ͼ����ʾ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
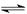 pC(��)��ƽ������������С��ԭ����
pC(��)��ƽ������������С��ԭ����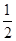 �����ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ����1.9������ѹ�������б����¶Ȳ��䣬��Ӧ����ʽ������ϵ����ϵ�ǣ� ��
�����ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ����1.9������ѹ�������б����¶Ȳ��䣬��Ӧ����ʽ������ϵ����ϵ�ǣ� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��MnO2�ܼ���H2O2�ķֽ⣬����ΪMnO2���Խ��ͷ�Ӧ����Ļ�� |
| B�����ɫ��K2Cr2O7��Һ�еμ�NaOH��Һ,��Һ��ɫ���,˵����ѧƽ�ⷢ�����ƶ� |
| C����NO2��N2O4��������ƽ����ϵ��ѹ��������������ɫ�����һ��ʵ��������������ԭ������ |
D�����ܱ������У����ڷ�Ӧ2A(g)+B(g) 2C(g)������ѹǿ��ƽ��������ƽ����Է���������С 2C(g)������ѹǿ��ƽ��������ƽ����Է���������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
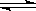 nC(g)�ķ�Ӧ��ϵ�У�C�İٷֺ���(c%)��ʱ��t����������ͼ��ʾ�����������ȷ����
nC(g)�ķ�Ӧ��ϵ�У�C�İٷֺ���(c%)��ʱ��t����������ͼ��ʾ�����������ȷ����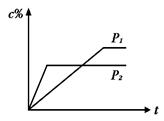
| A��P1��P2��n��3 | B��P1��P2��n��3 |
| C��P1��P2��n��3 | D��P1��P2��n��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2B(g) ��2A(g)
2B(g) ��2A(g) B(g)��ת���ʣ����¶Ȳ��������£�������A�����ʵ����������ж���ȷ���ǣ� ��
B(g)��ת���ʣ����¶Ȳ��������£�������A�����ʵ����������ж���ȷ���ǣ� ��| A��a1��a2����С | B��a1��a2������ |
| C��a1����a2��С | D��a1��С��a2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
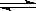 HClO��OH�������д�ʩ�������Ư��Ч�����( )
HClO��OH�������д�ʩ�������Ư��Ч�����( )| A����ˮϡ�� | B��ͨ��CO2 | C������������ | D��������NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 bB(g)�ﵽƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��B��Ũ����ԭ����60������ ( )
bB(g)�ﵽƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��B��Ũ����ԭ����60������ ( )| A��ƽ�����淴Ӧ�����ƶ��� | B������A��ת���ʼ�С�� |
| C������B���������������� | D��a>b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
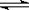 x C(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��Ϊ0.4mol/L���ݴ���д���¿հף�
x C(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��Ϊ0.4mol/L���ݴ���д���¿հף��鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com