
| A.元素周期律的本质是随着核电荷数的增加元素化合价呈周期性的变化 |
| B.核外电子排布的周期性变化是元素性质周期性变化的本质 |
| C.元素周期表中可以把元素分成s、p、d、ds 四个区 |
| D.元素周期表中最外层电子数≤2的元素一定是金属元素 |
科目:高中化学 来源:不详 题型:单选题
| A.同一周期中,碱金属元素的第一电离能最大 |
| B.同周期元素中,ⅦA族元素的原子半径最大 |
| C.当各轨道处于全满、半满、全空时原子较稳定 |
| D.ⅥA族元素的原子,其半径越大,越容易得到电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HXO4 | B.H2YO4 | C.H3ZO4 | D.H4WO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
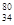 Se。下列有关该同位素的说法正确的是( )
Se。下列有关该同位素的说法正确的是( )| A.质子数为80 | B.电子数为114 | C.中子数为46 | D.质量数为34 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X、Y一定不是同周期元素 |
| B.X2+的氧化性一定大于Y+ |
| C.由mXa-与nYb+得,m-a=n+b |
| D.若气态氢化物的稳定性HmX大于HnY,则m>n |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高正化合价 | | +2 | +1 | +5 | +7 | +1 | +5 |
| 最低负化合价 | -2 | | | -3 | -1 | | -3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 I。
I。 I发射的射线可杀伤一部分甲状腺细胞,医疗上常采用其治疗甲状腺机能亢进。下列有
I发射的射线可杀伤一部分甲状腺细胞,医疗上常采用其治疗甲状腺机能亢进。下列有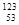 I
I  I
I  I
I  I的说法中正确的是
I的说法中正确的是| A.是同一种核素 | B.互为同素异形体 |
| C.互为同位素 | D.核外电子数和性质均相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com