
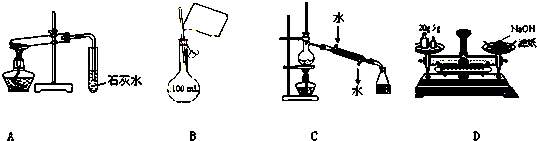
| A、装置探究NaHCO3的热稳定性 |
| B、配制100 mL 0.10 mol?L-1NaCl溶液 |
| C、实验室用该装置制取少量蒸馏水 |
| D、称量25 g NaOH |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
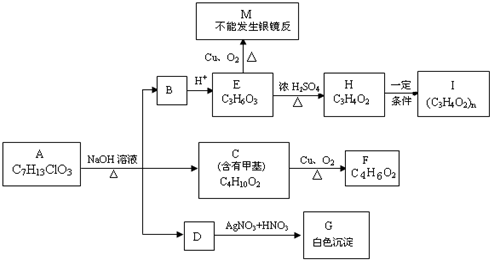
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(Min) 浓度(mol?L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
查看答案和解析>>
科目:高中化学 来源: 题型:
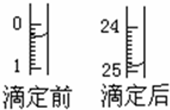 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定法测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定法测定其浓度.| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | 25.00 | 0.50 | 24.95 | 24.45 |
| 2 | 25.00 | |||
| 3 | 25.00 | 6.00 | 30.55 | 24.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:
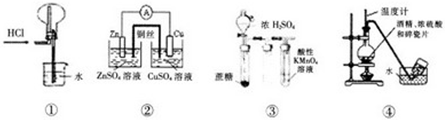
| A、实验①,氯化氢气体的吸收 |
| B、实验②,铜锌原电池 |
| C、实验③:酸性KMnO4溶液中出现气泡,且颜色不变 |
| D、实验④:实验室制取收集乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某溶液中滴加盐酸酸化的氯化钡溶液 | 出现白色沉淀 | 该溶液中一定存在SO42 |
| B | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | -两者均能与盐酸反应 |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 上层溶液 显紫红色 | 氧化性:Fe3+>I2 |
| A、A | B、B | C、C | D、D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2+3H2?2NH3 |
| B、H2 (g)+I2 (g)?2HI(g) |
| C、2NO2?N2O4 |
| D、HCl+NaOH?NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HBr |
| B、HCl |
| C、H2 |
| D、Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-o |
| 键能(Kj/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com