
����Ŀ����(N2H4)��һ��Ӧ�ù㷺�Ļ���ԭ�ϡ���ҵ���Ⱥϳɰ�����N2(g)+3H2(g) ![]() 2NH3(g)+Q(Q��0)���ٽ�һ���Ʊ��¡����������գ�
2NH3(g)+Q(Q��0)���ٽ�һ���Ʊ��¡����������գ�

��1���ϳɰ���Ҫѡ����ʵĴ���,�ֱ�ѡ��A��B��C���ִ�����������,���ý����ͼ��ʾ(����������ͬ)��������������ѡ��Ĵ�����___(�A����B����C��)�������ǣ�________________��
��2��һ�������£������ܱ������н��еĺϳɰ���Ӧ��ƽ���������������ʱ,��ͬʱѹ������������������¶ȴ���ƽ�����ԭƽ����ȣ��뽫�й��������ı仯����������±���(���������С������ȷ����)
��Ӧ���� | ƽ�ⳣ��K | ����������� | |
�仯��� | __ | ____ | ____ |
��3���¿���Ϊ���ȼ�ϣ�4gN2H4(g)��NO2������ȼ�����ɵ�������̬ˮ���ų�71kJ��������д���÷�Ӧ�Ļ�ѧ����ʽ��________��
��4������Ҫ�����������ʺ����ᡣ��ʮ���塱�ڼ䣬Ԥ���ҹ��ϳɰ�����������������������ͼ�Dz�ͬ�¶ȺͲ�ͬѹǿ��,��Ӧ�ﵽƽ���,�������NH3����(���%)�ı仯�������֪��ʼʱn(N2)��n(H2)=1:3���ж�pl��p2ѹǿ�Ĵ�С��ϵ��pl___p2(ѡ���������������=��)��
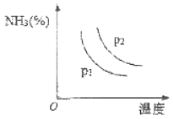
���𰸡�A �ڽϵ��¶��¾߱��ϸߵĴ����ԣ�һ����ɽ�Լ��Դ����һ������������ڷ�Ӧ��ת�� ���� ��С ��С 2N2H4(g)+2NO2(g)��3N2(g)+4H2O(g)+1136kJ �ϳɰ�Ϊ���������С�ķ�Ӧ,ѹǿԽ�����ĺ���Խ��,����ͼ���֪,�¶���ͬʱp2�����°����ĺ����ϸ�,��pl��p2ѹǿ�Ĵ�С��ϵΪpl��p2
��������
��1��ͼ�������֪����A�ķ�Ӧ���ʼӿ�ı������¶ȵͣ�
��2��������������ʱ����ͬʱѹ������������������¶ȴ���ƽ���N2��g��+3H2��g��2NH3��g��+Q��Q��0������ӦΪ���������С�ķ��ȷ�Ӧ������ѹǿƽ��������У������¶�ƽ��������У�ƽ�ⳣ�����¶ȱ仯��
��3��4gN2H4��g����NO2������ȼ�����ɵ�������̬ˮ���ų�71kJ���������ݴ���д��ѧ����ʽ��
��4�����ݷ�Ӧ�ķ���ʽ�жϣ�����ѹǿ��ƽ�������ƶ���
(1)�ϳɰ���Ҫѡ����ʵĴ������ֱ�ѡ��A��B��C���ִ����������飬���д���A�ڽϵ��¶��¾߱��ϸߵĴ����ԣ�һ����ɽ�Լ��Դ����һ������������ڷ�Ӧ��ת�����ʴ�Ϊ��A���ڽϵ��¶��¾߱��ϸߵĴ����ԣ�һ����ɽ�Լ��Դ����һ������������ڷ�Ӧ��ת����
(2)һ�������£������ܱ������н��еĺϳɰ���Ӧ��ƽ���������������ʱ����ͬʱѹ������������������¶ȴ���ƽ�����ԭƽ����ȣ���Ӧ���������¶�����Ӱ��ƽ��ij̶Ƚϴ�ƽ��������У�ƽ�ⳣ����С���������������С���ʴ�Ϊ������С����С��
(3)4gN2H4(g)��NO2������ȼ�����ɵ�������̬ˮ,�ų�71kJ������,2mol����ȫ��Ӧ����=71kJ��2��32/4=1136kJ���Ȼ�ѧ����ʽΪ2N2H4(g)+2NO2(g)��3N2(g)+4H2O(g)+1136kJ��
(4)�ϳɰ�Ϊ���������С�ķ�Ӧ��ѹǿԽ�����ĺ���Խ�ߣ�����ͼ���֪���¶���ͬʱp2�����°����ĺ����ϸ�,��pl��p2ѹǿ�Ĵ�С��ϵΪpl��p2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�д��ڵ���ƽ��CH3COOH![]() H����CH3COO��������ȷ���ǣ� ��
H����CH3COO��������ȷ���ǣ� ��
A. ������Һ������Ũ�ȵĹ�ϵ���㣺c��H������c��OH������c��CH3COO����
B. ������0.10mol/L��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��OH������С
C. CH3COOH��Һ�м�������CH3COONa���壬ƽ�������ƶ�
D. ������pH��2��CH3COOH��Һ��pH��12��NaOH��Һ�������Ϻ���Һ��pH��7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������NaOH��������1.0molL-1��NaOH��Һ230mL��
��1��������Һʱ��һ����Է�Ϊ���¼������裺��������пո�
A.���㣻B.������C.___��D.��ȴ��E.��Һ��F.___��G.���ݣ�H.ҡ�ȡ�װƿ��
��2����ʵ������õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ���Ͳ������___mL����ƿ��ʹ������ƿǰ������е�һ��������___��
��3�������___g�ռ���壬����Ӧ�÷���___�г�����
��4�������ƹ����У���������������ȷ�ģ����в���������Ũ��ƫ�ߵ���___��
A.û��ϴ���ձ��Ͳ�����
B.ת����Һʱ������������������ƿ����
C.����ƿ�����������������ˮ
D.����ʱ���ӿ̶���
E.δ��ȴ�����¾ͽ���Һת�Ƶ�����ƿ������
��5��������������Һȡ��100mL���ٽ���100mL��Һ��ˮϡ�ͳ�1L����Һ����ϡ�ͺ�������Һ�����ʵ���Ũ��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ������Ĺؼ���Ӧ�Ƕ������������Ϊ���������䷴Ӧ����ʽ2SO2g)+O2(g)![]() 2SO3(g)���ش������й����⣺
2SO3(g)���ش������й����⣺
��1������˷�Ӧ��������ʾ�Ļ�ѧ��Ӧ������v(O2)=0.05mol/(L��s),���ö��������ʾ��v(SO2)=______________.
��2�������������䣬�������¶ȣ��˷�Ӧ�����淴Ӧ�����ƶ���������Ӧ����______________���淴Ӧ����______________����������С��������Ӧ��______________��Ӧ�������Ȼ���ȣ���
��3�������������䣬����������Ũ�ȣ���ʹSO2��ת����______________��
��4�����������ܹ��жϴ˷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬����______________
A.��λʱ��������1molSO2��ͬʱ����1molSO3
B.���º�����������ϵ����ѹǿ������ʱ��ı仯���仯
C.���º��������»��������ܶȲ�����ʱ��ı仯���仯
D.2v(O2)��= v(SO2)��ʱ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ի�����Ϊԭ���Ʊ������ϩ�ĺϳ�·�ߣ�
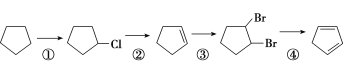
(1)��Ӧ�ٵIJ���������________����Ӧ�Ļ�ѧ����ʽΪ___________________��
(2)��Ӧ�ڵķ�Ӧ�Լ��ͷ�Ӧ������________����Ӧ�۵ķ�Ӧ������________��
(3)![]() ��NaOHˮ��Һ��Ӧ�Ļ�ѧ����ʽ________________________��
��NaOHˮ��Һ��Ӧ�Ļ�ѧ����ʽ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��H2(g)��I2(g)��Ӧ����HI(g)������ʾ��ͼ����ͼ��֪

A.�÷�Ӧ�����ȷ�Ӧ
B.1 mol HI(g)�ֽ����յ�����ΪQ
C.�Ȼ�ѧ����ʽ��H2+I2![]() 2HI+Q
2HI+Q
D.��Ӧ������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A~D����ѧʵ���г����ļ����¶ȼ�װ��ʾ��ͼ��
��1�������~����ѡȡ������ʹ���¶ȼƵ�ʵ�飬ѡ��A��Bװ���ʺϵ�ʵ����д�ո�
���ƾ���Ũ�����ϼ�������ϩ������ʯ��ˮ��Ӧ����Ȳ��������������������Ļ������������ȡ����Ӧ����ʯ�ͷ���ʵ�飬��Ũ����Ͷ������̻�ϼ���������
A | B | C |
|
|
|
_____________ | ___________ |
����Ũ����;ƾ��Ļ��˳��Ϊ_________________________��д��ʵ��������ϩ�Ļ�ѧ����ʽ____________________________��
����Ϊ�˻���ȶ�����������___________����ˮ��д��ʵ��������Ȳ�Ļ�ѧ����ʽ___________________________________��
��2��ѡ��װ��C����������ʵ�飬D�г������ܵ�������_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25���101kPaʱ�����顢��Ȳ�ͱ�ϩ��ɵĻ����20mL�������������ϲ���ȫȼ�գ���ȥˮ�������ָ���ԭ�����¶Ⱥ�ѹǿ�������������С��40mL��ԭ���������Ȳ���������Ϊ ( ��)
A. 12.5%B. 25%C. 50%D. 75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(a)����һ���°���»�Դ���ձ����Ҳ�Ƕ�����ж�������һ��ǿ�°������(a)�ŵĽṹ��ʽ��ͼ��ʾ�������йر���(a)�ŵ�˵���в���ȷ����(����)
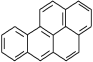
A. ����(a)�ŵķ���ʽΪC20H12�����ڳ���������
B. ����(a)����![]() ��Ϊͬ���칹��
��Ϊͬ���칹��
C. ����(a)����һ�������¿��Է���ȡ����Ӧ��������ʹ����KMnO4��Һ��ɫ
D. ����(a)�Ų�������ˮ�������ڱ����ȷµ��л��ܼ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com