
【题目】合成某药物的中间体G的流程如图:

请回答下列问题:
(1)A的名称为___(系统命名法),F的分子式为___。反应⑤的反应类型是___。
(2)C中含氧官能团的名称为__。
(3)已知一定条件下2分子乙酸分子间脱水生成1分子乙酸酐,写出该反应的化学方程式:___。
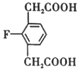
(4)写出满足下列条件的E的同分异构体的结构简式:___。
①苯环上只有三个取代基;
②核磁共振氢谱图中只有4组吸收峰;
③1mol该物质与足量NaHCO3溶液反应生成2molCO2。
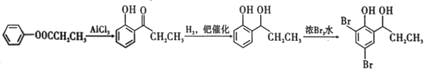
(5)根据已有知识并结合相关信息,写出以C6H5—OOCCH2CH3为原料制备 的合成路线流程图(无机试剂任选)。___。
的合成路线流程图(无机试剂任选)。___。
【答案】4-氟苯酚 C10H7O3F 消去反应 羰基(酮基)、(酚)羟基 2CH3COOH ![]() CH3COOCOCH3+H2O
CH3COOCOCH3+H2O 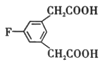 、
、
【解析】
①![]() 在浓硫酸作用下与乙酸酐发生取代反应生成B
在浓硫酸作用下与乙酸酐发生取代反应生成B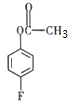 ,②B在氯化铝催化作用下异构为C
,②B在氯化铝催化作用下异构为C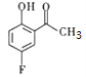 ,③C与乙二酸二乙酯反应生成D
,③C与乙二酸二乙酯反应生成D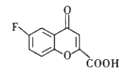 ,④D与氢气在钯催化作用下发生加成反应生成E
,④D与氢气在钯催化作用下发生加成反应生成E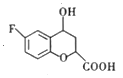 ,⑤E发生消去反应生成F
,⑤E发生消去反应生成F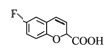 ,⑥F与氢气发生加成反应生成G
,⑥F与氢气发生加成反应生成G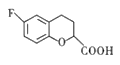 。
。
(1)A![]() 的名称为4-氟苯酚(系统命名法),F的结构简式为
的名称为4-氟苯酚(系统命名法),F的结构简式为 ,分子式为C10H7O3F。E为
,分子式为C10H7O3F。E为 ,⑤E发生消去反应生成F
,⑤E发生消去反应生成F ,反应⑤的反应类型是消去反应。故答案为:4-氟苯酚;C10H7O3F;消去反应;
,反应⑤的反应类型是消去反应。故答案为:4-氟苯酚;C10H7O3F;消去反应;
(2)C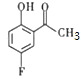 中含氧官能团的名称为羰基(酮基)、(酚)羟基。故答案为:羰基(酮基)、(酚)羟基;
中含氧官能团的名称为羰基(酮基)、(酚)羟基。故答案为:羰基(酮基)、(酚)羟基;
(3)一定条件下2分子乙酸分子间脱水生成1分子乙酸酐,该反应的化学方程式:2CH3COOH ![]() CH3COOCOCH3+H2O。故答案为:2CH3COOH
CH3COOCOCH3+H2O。故答案为:2CH3COOH ![]() CH3COOCOCH3+H2O;
CH3COOCOCH3+H2O;
(4)E为 ,不饱和度为6,满足下列条件的E的同分异构体:①苯环上只有三个取代基,除苯环外,还有2个不饱和度;②核磁共振氢谱图中只有4组吸收峰,分子对称;③1mol该物质与足量NaHCO3溶液反应生成2molCO2,分子中有两个羧基,满足条件的结构简式为:
,不饱和度为6,满足下列条件的E的同分异构体:①苯环上只有三个取代基,除苯环外,还有2个不饱和度;②核磁共振氢谱图中只有4组吸收峰,分子对称;③1mol该物质与足量NaHCO3溶液反应生成2molCO2,分子中有两个羧基,满足条件的结构简式为: 、
、 ;故答案为:
;故答案为: 、
、 ;
;
(5)比较C6H5—OOCCH2CH3原料和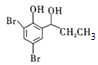 ,苯环不变,碳原子数不变,根据②B
,苯环不变,碳原子数不变,根据②B 在氯化铝催化作用下异构为C
在氯化铝催化作用下异构为C 的相关信息,以C6H5—OOCCH2CH3为原料先制备
的相关信息,以C6H5—OOCCH2CH3为原料先制备![]() ,再用钯催化用氢气将羰基还原为羟基,最后与浓溴水发生取代反应得
,再用钯催化用氢气将羰基还原为羟基,最后与浓溴水发生取代反应得 ,合成路线流程图(无机试剂任选)如下:
,合成路线流程图(无机试剂任选)如下: 。故答案为:
。故答案为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.氯气通入水中,溶液呈酸性:Cl2 + H2O ![]() 2H+ + Cl-+ ClO-
2H+ + Cl-+ ClO-
B.向氯化铝溶液中加入过量氨水: Al3+ + 4OH-=AlO2-+ 2H2O
C.碳酸氢铵溶液中加足量的氢氧化钠溶液:NH4+ + OH- = NH3↑ + H2O
D.二氧化硫通入溴水中,溴水褪色:SO2 + Br2 + 2H2O = 4H+ + 2Br- + SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g) ![]() CH4(g)+2O2(g) ΔH=+802KJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线。下列说法正确的是
CH4(g)+2O2(g) ΔH=+802KJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线。下列说法正确的是
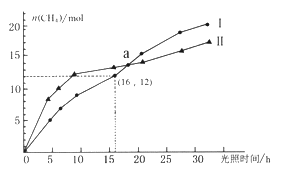
A. 0-15h内,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好
B. 反应开始后的30h内,第Ⅰ种催化剂的作用下,反应吸收的热量多
C. a点时,CO2的转化率相等
D. 0-16h内,v(O2)=1.5mol/(L·h)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家。有两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂为正极的磷酸铁锂电池。请回答下列问题:
(1)基态钴原子的价电子排布式为____,Mn位于元素周期表的____ 区(填“s”或“p”或“d”或“ds”或“f”)。
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是___。PO43-的空间构型是 ___,中心原子的杂化方式是 ____。
(3)CoO、MnO两种氧化物的熔点由高到低的顺序是 ___,原因是 ___。
(4)PH3是____分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是 _____
(5)硫化锂Li2S(摩尔质量Mgmol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag.cm-3,则距离最近的两个S2-的距离是___nm。(用含a、M、NA的计算式表示)
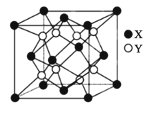
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25°C时有关弱酸的电离平衡常数如下表:
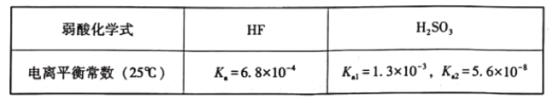
下列有关说法正确的是( )
A.等物质的量浓度的各溶液pH关系:pH(Na2SO3)<pH(NaF)<pH(NaHSO3)
B.将0.lmo/L的HF与0.1mol/L的NaF等体积混合,混合液pH>7
C.Na2SO3溶液中加入足量HF发生反应的离子方程式为SO32-+HF=F-+HSO3-
D.NaHSO3溶液中部分微粒浓度的大小:c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知铜在常温下能被HNO3溶解。反应方程式为: 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目_______。
(2)若生成0.2mol的NO,则该过程中转移的电子是___________mol。
(3)被还原的硝酸占参加反应硝酸的比例为___________。
Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→ O2,写出该化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒温恒容密闭容器中存在反应:X(g)+2Y(g) ![]() Z(g) ΔH=-a kJmol-1(a>0),现向该容器中充入等物质的量的X(g)与Y(g)充分反应。下列说法正确的是
Z(g) ΔH=-a kJmol-1(a>0),现向该容器中充入等物质的量的X(g)与Y(g)充分反应。下列说法正确的是
A.体系中混合气体的平均摩尔质量保持不变时,说明该反应达到化学平衡状态
B.达到平衡时,反应放出的热量一定小于a kJ
C.达到平衡时,X与Y的物质的量之比仍为1∶1
D.达到平衡后,若升高体系温度,则逆反应速率增加、正反应速率减少,平衡逆移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2
实验流程如下:
C6H12O6溶液![]()
![]()
![]() 滤液
滤液![]() 悬浊液
悬浊液![]()
![]()
![]() Ca(C6H11O7)2
Ca(C6H11O7)2
已知:葡萄糖酸钙微溶于乙醇,可溶于冷水,易溶于热水。则下列说法不正确的是
A.第②步充分反应后CaCO3固体需有剩余,其目的是确保葡萄糖酸完全转化为钙盐
B.第④步加入乙醇的作用是减小葡萄糖酸钙在水中的溶解量,使其结晶析出
C.第⑤步过滤时,发现有固体产品残留在原容器壁上,可加少量热水冲洗再转移至过滤器内
D.可用O2代替Br2,在葡萄糖氧化酶作用下氧化葡萄糖进而制备葡萄糖酸钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com