
【题目】在4L密闭容器中充入6molA气体和5molB气体,在一定条件下发生反应:3A(g)+B(g)![]() 2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol·L-1,试计算:(写出简单的计算过程)
2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol·L-1,试计算:(写出简单的计算过程)
(1)x的值为多少________
(2)B的转化率为多少________
(3)平衡时A的浓度为多少________
科目:高中化学 来源: 题型:
【题目】将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:SO2+2Fe3++2H2O = SO42+4H++2Fe2+,Cr2O72+6Fe2++14H+ = 2Cr3++6Fe3++7H2O。下列说法正确的是( )
A.还原性:Cr3+>Fe2+>SO2B.氧化性:Cr2O72>Fe3+>SO2
C.Cr2O72不能将SO2氧化D.两个反应中Fe2(SO4)3均作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
A. 0.4mol
B. 0.2mol
C. 小于0.2mol
D. 大于0.2mol,小于0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在体积为5L的密闭容器中发生某可逆反应,其化学平衡常数表达式为:K=![]() 。
。
(1)请写出该反应的化学方程式:___。
(2)恒温恒容条件下容器中气体的平均相对分子质量、气体的分子总数或混合气体的___不再随时间变化,都可说明该反应已达平衡状态。
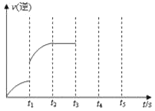
(3)该反应的逆反应速率随时间变化的关系如图,t1时的突变一定是因为某种条件的改变,该改变不可能是___;
a.减小H2浓度 b.使用催化剂 c.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2A![]() B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20分钟内A的平均速率为____________。
(2)在实验2中,A的初始浓度=_____,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是____。
(3)设实验3中的反应速率为v3,实验1的反应速率为v1,则v3______v1(填“>”、“=”或“<”),且C3___1.0mol/L(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应是____反应(填“吸热”或“放热”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞香素具有消炎杀菌作用,结构如图所示,下列叙述正确的是
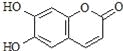
A.与稀H2SO4混合加热不反应
B.不能使酸性高锰酸钾溶液褪色
C.1mol 瑞香素最多能与3mol Br2发生反应
D.1mol瑞香素与足量的NaOH溶液发生反应时,消耗NaOH 3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大多数金属硫化物难溶于水,可溶于硝酸。例如:
①FeS +HNO3(稀)→Fe(NO3)3 +NO↑+S↓+H2O(未配平)
②CuS +HNO3(浓)→CuSO4 +NO2↑+H2O(未配平)
(1)配平反应②的方程式:
__CuS +__HNO3(浓)→__CuSO4 +__NO2↑+__H2O
(2)反应①中若生成3.2g硫,则电子转移___个。
(3)由反应①和②是否能够判断稀硝酸与浓硝酸的氧化性强弱?并说明判断依据。____。
(4)反应①和②所涉及的4种非金属元素中,原子半径由大到小的顺序是____;未成对电子最多的原子核外电子排布式为___。
下列描述,不能用来比较硫、氮两种元素的非金属性强弱的是___。
a.单质与氧气化合的难易程度 b.气态氢化物的稳定性
c.含氧酸的酸性强弱 d.S4N4中共用电子对的偏向
(5)写出①NO ②S ③H2O ④NO2四种物质的沸点由高到低的顺序(用编号回答)____。若要判断NO2分子的极性,你所需要的信息是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为短周期元素,A、B、C在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。D与A同周期,其最高正价与最低负价代数和为零。A、E可形成AE3型分子,分子中只存在极性键。
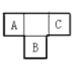
(1)B元素在元素周期表中的位置是____________________。
(2)C的离子结构示意图为__________________,用电子式表示AE3的形成过程:_______________________________________。
(3)由元素A、C及氢元素形成的化合物中含有的化学键的类型有____________。
(4)请设计一个实验来说明D与A的非金属性强弱(写出化学方程式即可)_________________在铜锌硫酸原电池中,若负极减少是13g,则正极产生__________升气体(标准状况)?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A. 原子半径:A>B>D>CB. 原子序数:d>c>b>a
C. 离子半径:C>D>B>AD. 单质的还原性:A>B>D>C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com