

���� ��1��װ��A��������������Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�������
��2���ٰ���A��C��F˳������װ�ã����б��͵����������Ƴ�ȥHCl����������ͨ����������Һ������������ԭ��Ӧ��
�ڴ��������ǿ�����ԡ�����������л�ԭ�ԣ��������ö���������������ֱ�ӷ�Ӧ�ж�������������������ǿ��������֤���������Ա�̼��ǿ���ٽ��̼�����Ա�HClOǿ�����жϣ�Aװ���Ʊ������������������ӷ����Ʊ��Ķ��������л���HCl���ñ��͵����������Ƴ�ȥHCl����ͨ��̼��������Һ��������֤���������Ա�̼��ǿ�������Ը��������Һ������ȥ������̼�еĶ���������Ʒ����Һ���������̼�ж��������Ƿ��������ͨ��F�У�
��3���ٸ�װ��������C������Ϊ���������ܣ���ȡ����ԭ��ͨ������ˮ��
�ڸ��ݹ�ϵʽ��10I-+2MnO4-+16H+=2Mn2++5I2+8H2O���������KMnO4���ٸ���5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+�����Һ��SO2�ĺ�����
��� �⣺��1��װ��A��������������Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ����������ӷ���ʽΪ��2H++CaSO3=Ca2++H2O+SO2����
�ʴ�Ϊ��2H++CaSO3=Ca2++H2O+SO2����
��2���ٰ���A��C��F˳������װ�ã����б��͵����������Ƴ�ȥHCl����������ͨ����������Һ������������ԭ��Ӧ������֤��ǿ���Ʊ������ԭ��������֤��������ʹ����������ǿ����
�ʴ�Ϊ����������ͨ����������Һ������������ԭ��Ӧ����֤��ǿ���Ʊ������ԭ����
�ڴ��������ǿ�����ԡ�����������л�ԭ�ԣ��������ö���������������ֱ�ӷ�Ӧ�ж�������������������ǿ��������֤���������Ա�̼��ǿ���ٽ��̼�����Ա�HClOǿ�����жϣ�Aװ���Ʊ������������������ӷ����Ʊ��Ķ��������л���HCl���ñ��͵����������Ƴ�ȥHCl����ͨ��̼��������Һ��������֤���������Ա�̼��ǿ�������Ը��������Һ������ȥ������̼�еĶ���������Ʒ����Һ���������̼�ж��������Ƿ��������ͨ��F�У���װ������˳��ΪA��C��B��E��D��F������װ��C�������dz�ȥHCl���壬D��Ʒ�첻��ɫ��F�г��ְ�ɫ��������֤�������������ǿ�ڴ����ᣬ
�ʴ�Ϊ��B��E��D��F����ȥHCl��������Ӱ������ʵ���ã�װ��D��Ʒ�첻��ɫ��F�г��ְ�ɫ������
��3���ٸ�װ��������C������Ϊ���������ܣ���ȡ����ԭ��ͨ������ˮ�������������ܽ�ˮ��Ϊb��
�ʴ�Ϊ�����������ܣ�b��
����10I-+2MnO4-+16H+=2Mn2++5I2+8H2O���������KMnO4���ʵ���Ϊ$\frac{1}{5}$��0.200Omol/L��0.025L=0.001mol��
�������Һ��SO2��Ӧ��KMnO4���ʵ���Ϊ0.02L��0.1000mol/L-0.001mol=0.001mol��
��5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+�����Һ��SO2����Ϊ0.001mol��$\frac{5}{2}$=0.0025mol�����Բ�Һ��SO2�ĺ���Ϊ=$\frac{0.0025mol}{0.01L}$=0.25mol/L��
�ʴ�Ϊ��0.25��
���� ���⿼�������Ʊ�������ʵ�顢���ʺ����ⶨʵ�飬�漰װ�÷��������ۡ�ʵ�鷽����ơ�����ʹ�á���ѧ����ȣ��ؼ�����ȷʵ��ԭ�����ϺõĿ���ѧ��ʵ���ۺ�������֪ʶǨ��Ӧ�ã��Ѷ��еȣ�


 �Űٷֿ�ʱ����ϵ�д�
�Űٷֿ�ʱ����ϵ�д� ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��A�������������Se�����ڣ�Te����Ԫ���ڻ������г����ֳ����ֻ��ϼۣ�����A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⣺
��A�������������Se�����ڣ�Te����Ԫ���ڻ������г����ֳ����ֻ��ϼۣ�����A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
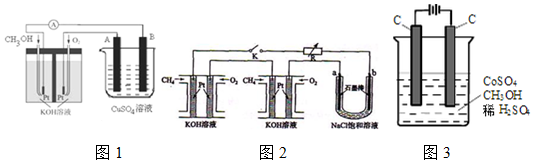
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
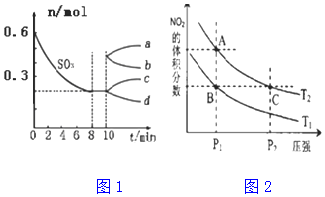
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ��ʯī | B�� | ��ˮ����� | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
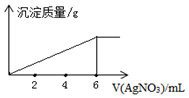
| A�� | +1 | B�� | +2 | C�� | +3 | D�� | +4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NH3 | B�� | H2 | C�� | HCl | D�� | CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x+y��z | B�� | B��ת���ʽ��� | ||
| C�� | ƽ��������Ӧ�����ƶ� | D�� | C������������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com