
分析 (1)根据反应3Cl2+8NH3═6NH4Cl+N2结合产物回答实验现象;
(2)氯气可以和强碱氢氧化钙之间反应生成氯化钙、次氯酸钙和水,据此书写方程式;
(3)根据氧化还原反应中电子守恒以及元素守恒来计算即可.
解答 解:(1)根据反应3Cl2+8NH3═6NH4Cl+N2,会看到的实验现象是出现白烟,故答案为:出现白烟;
(2)氯气可以和强碱氢氧化钙之间反应生成氯化钙、次氯酸钙和水,方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液.过程中氯气既是氧化剂又是还原剂,当NaCl和NaClO3的物质的量之比为8:1时,Cl原子失电子是5mol,的电子是8mol,所以NaClO的物质的量是3mol,混合液中NaClO和NaClO3的物质的量之比为3:1,故答案为:3:1.
点评 本题考查学生物质的性质以及氧化还原反应中电子守恒的计算知识,注意知识的迁移应用是关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Na暴露于空气中最终生成Na2O2 | |
| B. | 铜粉能溶于酸性硝酸钠溶解 | |
| C. | Fe比Al更易与NaOH溶液反应生成H2 | |
| D. | 水蒸气通过灼热的铁粉会有红棕色固体生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中 Mg2+、Al3+、SO42-、CO32- | |
| B. | pH=1的溶液中 NH4+、Ba2+、HCO3-、NO3- | |
| C. | 含MnO4-的溶液中 H+、K+、Br-、I- | |
| D. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液中 Na+、K+、CH3COO-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
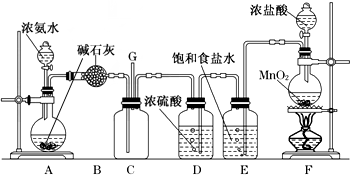
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
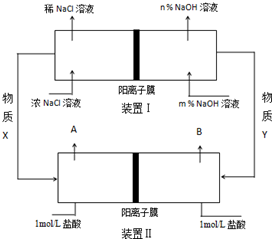
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在空气中,钢铁制品和铝制品都容易发生吸氧腐蚀 | |
| B. | 聚乙烯塑料易老化,是因为发生了加成反应 | |
| C. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 | |
| D. | 空气质量指标中有一项指标名称为PM2.5,指的是空气中直径≤2.5微米的固体或液体的总称 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com