
【题目】氯化氢可以用浓硫酸作用于氯化物来制取,主要是因为浓硫酸具是( )
A.强酸
B.高沸点酸
C.脱水剂
D.强氧化剂
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有碳等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是( )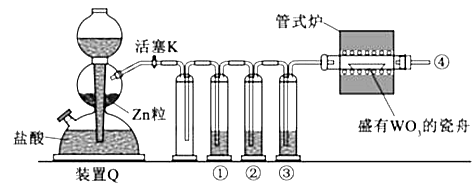
A.①、②、③中依次盛装KMNO4溶液、浓H2SO4、焦性没食子酸溶液
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体浓度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,CaC2O4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( ) 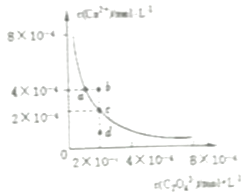
A.向CaC2O4饱和溶液中加入固体Na2C2O4可以由a点变到b点
B.通过蒸发可以由d点变到c点
C.d点无CaC2O4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3Cl为无色,略带臭味的气体,密度为2.25g/L,熔点为﹣24.2℃,不易溶于水,易溶于乙醇和丙醇等有机溶剂. Ⅰ.实验室制取CH3Cl的原理是CH3OH+HCl(浓) ![]() CH3Cl+H2O.具体步骤如下:
CH3Cl+H2O.具体步骤如下:
①干燥ZnCl2晶体;
②称取24g研细的无水ZnCl2和量取20mL浓盐酸放入圆底烧瓶,同时量取一定量的甲醇放入分液漏斗中;
③将分液漏斗里的甲醇逐滴滴入烧瓶中并加热,待ZnCl2完全溶解后有CH3Cl气体逸出,可用排水法收集.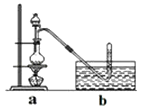
请回答:
(1)实验室干燥ZnCl2晶体制得无水ZnCl2的方法是
(2)反应过程中滴入烧瓶中甲醇的体积比盐酸少(甲醇与浓盐酸的物质的量浓度接近)其理由是 .
(3)实验室为何用排水法收集CH3Cl?
(4)Ⅱ.据某资料记载,CH4分子中的一个H原子被Cl原子取代后,其稳定性受到影响,可被强氧化剂酸性高锰酸钾氧化.现有四只洗气瓶;分别盛有以下试剂: A.1.5%KMnO4(H+)溶液; B.蒸馏水;C.5%Na2SO3溶液; D.98%H2SO4
为证实这一理论的可靠性,请从上面选择最恰当的洗气瓶,将a装置生成的气体依次通过洗气瓶(填洗气瓶编号),如果观察到则证实上述资料的正确性.
(5)写出洗气瓶中发生反应的离子方程式(C元素的氧化产物为CO2):
(6)如果CH3Cl是大气的污染物,上述洗气瓶之后还应接一只盛的洗气瓶.
(7)某小组同学取VmL被CH3Cl污染的水样与锥形瓶中,用0.10molL﹣1酸性KMnO4溶液进行滴定,实验所得数据如表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.90 | 20.02 | 20.00 | 19.98 |
第一次实验数据出现异常,造成这种异常的原因可能是(填字母代号).
a.锥形瓶洗净后未干燥 b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定过程中振荡锥形瓶时有液体溅出 d.滴定终点时仰视读数.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】接触法制硫酸工艺中,其主反应是在恒容、温度为450℃并有催化剂存在的条件下进行:2SO2(g)+O2(g)2SO3(g)△H=﹣190kJ/mol ①下列描述中能说明上述反应已达平衡的是 .
a.v(O2)正═2v(SO3)逆 b.容器中气体的密度不随时间而变化
c.容器中气体的平均相对分子质量不随时间而变化 d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2 , 半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=molL﹣1min﹣1 , 若继续通入0.40mol SO2和0.20molO2则平衡移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,mol<n(SO3)<mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“ ![]() ”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
A.Ts是第七周期第ⅦA族元素
B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱
D.中子数为176的TS核素符号是 ![]() Ts
Ts
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列冶炼金属的方法正确的是( )
A.电解MgO制取Mg
B.加热条件下用CO还原Ag2O制取Ag
C.在Al和F2O3反应中,生成11.2gFe,转移电子数为0.6NA
D.电解NaCl溶液制取Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )
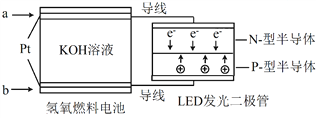
A. 电路中的电子从负极经外电路到正极,再经过KOH溶液回到负极,形成闭合回路
B. a处通入氢气, b处通氧气,该装置将化学能最终转化为电能
C. 电池放电后, OH-的物质的量浓度减小
D. 通入O2的电极发生反应:O2 + 4e- = 2O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某周期ⅡA族元素的原子序数为 x,则同周期的第ⅢA族元素的原子序数是( )
A.只有 x+1
B.可能是 x+8或 x+18
C.可能是 x+2
D.可能是 x+1或 x+11或x+25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com