
����Ŀ���Ӵ��������Ṥ���У�������Ӧ���ں��ݡ��¶�Ϊ450�沢�д������ڵ������½��У�2SO2��g��+O2��g��2SO3��g����H=��190kJ/mol ��������������˵��������Ӧ�Ѵ�ƽ����� ��
a��v��O2�����T2v��SO3���� b��������������ܶȲ���ʱ����仯
c�������������ƽ����Է�����������ʱ����仯 d������������ķ�����������ʱ����仯
����һ���̶��ݻ�Ϊ5L���ܱ������г���0.20molSO2��0.10molO2 �� ����Ӻ�ﵽƽ�⣬��������к�SO30.18mol����v��O2��=molL��1min��1 �� ������ͨ��0.40mol SO2��0.20molO2��ƽ���ƶ����������Ӧ���������淴Ӧ�����������ٴδﵽƽ���mol��n��SO3����mol��
���𰸡�cd��0.036��������Ӧ����0.54��0.60
���������⣺��a���ԣ�O2����=2�ԣ�SO3���� �� ����֮�Ȳ����ڻ�ѧ������֮�ȣ��ʴ��� b������������������ܶ�һֱ����ʱ����仯��˵����Ӧ��һ����ƽ��״̬���ʴ���
c���������������Է�����������ʱ����仯��˵����������ʵ����ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
d������������ķ�����������ʱ����仯��˵����������ʵ������䷴Ӧ��ƽ��״̬������ȷ��
��ѡ��cd���ڵ�����0.18molSO3ʱ���μӷ�Ӧ�����������ʵ���Ϊx��
2SO2��g��+ | O2��g�� | 2SO3��g�� |
1 | 2 | |
x | 0.18mol |
x= ![]() =0.09mol
=0.09mol
v��O2��= ![]() =0.036mol��L��1min��1��
=0.036mol��L��1min��1��
����ͨ��0.40mol SO2��0.20mol O2 �� ������ѹǿ����ƽ�������������С�ķ����ƶ�����������Ӧ�����ƶ���
�ü������n��SO3���ķ�Χ��
����ƽ�ⲻ�ƶ�����ʱn��SO3��=0.18��3=0.54mol��
�����ʱ�ܵ�0.60molSO2��ȫ����SO3 �� ���ݷ�Ӧ����ʽ2SO2��g��+O2��g��2SO3��g����֪��n��SO3��=0.6mol��
�����ٴδﵽƽ��ʱ��0.54mol��n��SO3����0.60mol��
���Դ��ǣ�0.036��������Ӧ����0.54��0.60��
�����㾫�������û�ѧƽ��ļ������Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪��Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�1 molX��n mol Y�����Ϊ2L���ܱ������з������·�Ӧ��X��g��+Y��g��=2Z��g��+M��s����5min��ﵽƽ�⣬��ʱ����2a mol Z������˵����ȷ���ǣ� ��
A.��X��ʾ�˷�Ӧ�ķ�Ӧ�����ǣ�0.1��0.2a��mol��Lmin����1
B.�����������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬
C.��ƽ������ϵ�м���1mol M��ƽ�����淴Ӧ�����ƶ�
D.������ƽ����ϵ���ٳ���1mol X��v����������v���棩��С��ƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У������������ӵ���
A.�������ҺB.����������ҺC.Һ��D.��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����һ���״�ȼ�ϵ�أ����øõ�ص��200mLһ��Ũ�ȵ�NaCl��CuSO4�����Һ����װ����ͼ1�� 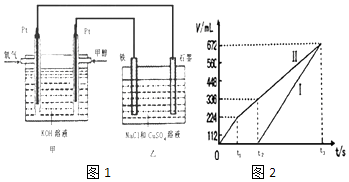
��1��д������ͨ��״���һ���ĵ缫��Ӧʽ ��
��2������������������������������ʱ��仯�Ĺ�ϵ��ͼ2��ʾ���ѻ���ɱ�״���µ��������д����t1��ʯī�缫�ϵĵ缫��Ӧʽ��ԭ�����Һ��NaCl�����ʵ���Ũ��Ϊmol/L��������Һ������䣩
��3������������װ����ͨ�����µ�����336mLʱ�������������缫�Ͽ�����ͭ������Ϊg��
��4����֪����H2C2O4Ϊ���ᣮ �ٳ����£�������ʵ��˵��������������ʵ��� ��
A�����������Һ�ӷ�̪����Һ���
B��ȡһ����������Һ��ˮϡ����10����pH�仯С��1
C��������ʹ����KMnO4��Һ��ɫ
D��ȡ��ͬpH�IJ�����Һ�����ᣬ�ֱ���������Ĵ�С����״��ͬ��þ����������Һ��Ӧ�ٶȿ�
�ڳ����£�0.1molL��1�IJ�����Һ��pH=13��NaOH��Һ�������ϣ�������Һ��pHΪ6����c��HC2O4��+2c��C2O42����=����ȷ����ѧ����ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������AlN��������ɰ�ּ�����¯�IJ��ϣ��ۻ�״̬�²����磬��֪�����ڣ� ��
A.���Ӿ���
B.ԭ�Ӿ���
C.���Ӿ���
D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ��������Ũ�����������Ȼ�������ȡ����Ҫ����ΪŨ������ǣ�������
A.ǿ��
B.�߷е���
C.��ˮ��
D.ǿ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڷ�Ӧ3Cl2��6KOH=5KCl��KClO3��3H2O�У����������뻹ԭ��������ʵ���֮��Ϊ�� ��
A. 1:3 B. 1:2 C. 1:5 D. 5:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����ڴ�������ǣ� ��
���մɣ���ˮ�࣬�۲�������Ư�ۣ��ݵ���������ˮ����Һ�ȣ�
A.�٢ۢ�
B.�ڢܢ�
C.�ݢ�
D.�ޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��2NO2![]() 2NO+O2�ں����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��( )
2NO+O2�ں����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��( )
����λʱ��������n molO2��ͬʱ����2n molNO2��
����λʱ��������n molO2��ͬʱ����2n mol NO��
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬��
�����������![]() ���䣻
���䣻
������������ɫ���ٸı��״̬��
�����������ܶȲ��ٸı��״̬��
����������ƽ����Է����������ٸı��״̬��
A. �٢ݢ� B. �٢ܢݢ� C. �٢ݢޢ� D. �٢ۢݢޢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com