
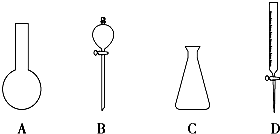
 根据常见仪器的特点及使用注意事项回答下列问题.
根据常见仪器的特点及使用注意事项回答下列问题.

 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
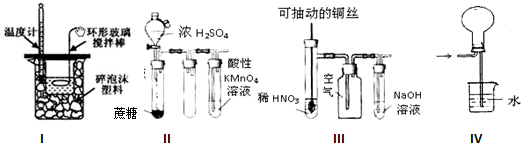
| A、实验I:中和热测定 |
| B、实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C、实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D、实验IV:可用于HCl气体的吸收 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com