
【题目】下列做法对人体健康不会造成危害的是( )
A.用工业盐(NaNO2)作咸味调味品
B.用硫磺熏制银耳,使它颜色更白
C.食盐中加入一定量的碘酸钾(KIO3)制取加碘食盐
D.将含有甲醇(CH3OH)的工业酒精兑制成饮用白酒
科目:高中化学 来源: 题型:
【题目】科学家最近在﹣100℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示,下列说法中不正确的是( ) 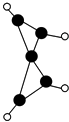
A.该分子的分子式为C5H4
B.该分子中碳原子的化学环境有2种
C.1mol X在一定条件下可与2mol H2发生反应
D.该分子中只有C﹣C键,没有C═C键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接氨硼烷(NH3·BH3)电池可在常温下工作,装置如图。该电池的总反应为:NH3·BH3+3H2O=NH4BO2+4H2O。下列说法正确的是( )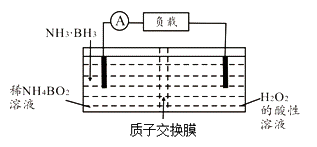
A.左侧电极发生还原反应
B.电池工作时,H+通过质子交换膜向负极移动
C.正极的电极反应式为2H++2e-=H2↑
D.消耗3.1g氨硼烷,理论上转移0.6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业采用氯化铵焙烧菱锰矿制备碳酸锰的流程如下图所示: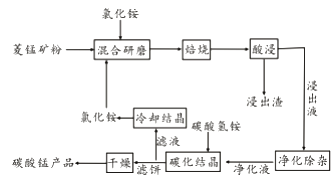
已知:①菱锰矿的主要成分是MnCO3 ,其中含Fe、Ca、Mg、Al等元素。
②焙烧过程中主要反应为:MnCO3 +2NH4Cl ![]() MnCl2+2NH3↑ +CO2↑+ H2O。
MnCl2+2NH3↑ +CO2↑+ H2O。
③部分阳离子沉淀时溶液的pH的值:
Al3- | Fe3+ | Ca2+ | Mn2+ | Mg2+ | |
开始沉淀的pH值 | 4.1 | 2.2 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH值 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
(1)实验室“焙烧”操作盛放固体的仪器为。
(2)结合图1、2、3,分析焙烧过程中对温度、NH4Cl用量[m(NH4Cl):m(锰矿粉)]、时间的最佳选择依次为、、。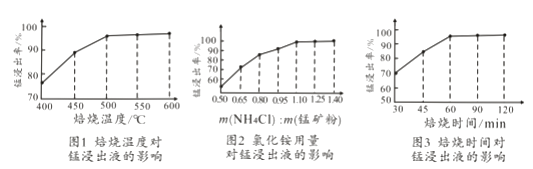
(3)对锰浸出液净化除杂时,先加入MnO2将Fe2+转化为Fe3+ , 再调节溶液pH的范围为 , 将Fe3+和Al3+变为沉淀除去。然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(4)“碳化结晶”步骤中,加入碳酸氢铵是反应的离子方程式为。
(5)上述流程中可循环使用的物质是。
(6)为测定产品中碳酸锰的含量,设计如下实验(杂质不参加反应):实验步骤为:称取16.80g试样,溶于适量的稀硫酸溶液中,向所得溶液中加入稍过量的磷酸和硝酸,加热使反应:2Mn2++NO3-+4PO43-+2H+ ![]() 2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+ , 滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+ , 滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为(还原产物是Cr3+)。
②产品中碳酸锰的质量分数为(结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物D的结构为 ![]() ,是一种常见的有机溶剂,它可以通过下列三步反应制得:烃A
,是一种常见的有机溶剂,它可以通过下列三步反应制得:烃A ![]() B
B ![]() C
C ![]() D,下列相关说法中正确的是( )
D,下列相关说法中正确的是( )
A.烃A为CH3CH3
B.反应②属于消去反应
C.反应①②③都属于取代反应
D.化合物D属于醚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四个试管中,发生如下反应:Zn+2HCl=ZnCl2+H2↑,产生H2的反应速率最小的是( )
试管 | 盐酸浓度 | 温度 | 锌的状态 |
A | 0.5molL﹣1 | 20℃ | 块 状 |
B | 0.5molL﹣1 | 20℃ | 粉末状 |
C | 2molL﹣1 | 35℃ | 块 状 |
D | 2molL﹣1 | 35℃ | 粉末状 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室进行氯气的制备及性质实验的组合装置,部分固定装置未画出。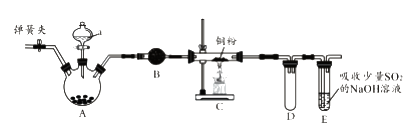
(1)A中固体是氯酸钾,液体a是浓盐酸,写出该反应的化学方程式:。
(2)B为干燥装置,加入的固体是;欲净化氯气,A、B间应添加一个盛有的洗气瓶。
(3)C中的反应现象是;D的作用是。
(4)已知E中发生的反应为:Cl2+Na2SO3+2NaOH ![]() 2NaCl+Na2SO4+H2O。E中吸收尾气一段时间后,吸收液(强碱性)中肯定存在:Cl-、OH-和SO42-。某兴趣小组认为该吸收液中还可能存在ClO-和SO32-。
2NaCl+Na2SO4+H2O。E中吸收尾气一段时间后,吸收液(强碱性)中肯定存在:Cl-、OH-和SO42-。某兴趣小组认为该吸收液中还可能存在ClO-和SO32-。
a.甲同学认为该吸收液中ClO-和SO32-不能同时存在,其理由是(用离子方程式表示)。
b.乙同学为了检验吸收液中是否含有SO32- , 取少量吸收液于试管中,加适量稀硫酸酸化后,滴加品红溶液,发现品红溶液褪色。据此推断该吸收液中一定有SO32-。乙同学的推断是否正确?(填“正确”或“不正确”),理由是。
c.请设计实验检验吸收液中是否含有ClO-(写出实验步骤、现象和结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCO3与砂搪混用可以作补血剂,实验室里制备FeCO3的流程如图所示。

下列说法错误的是
A. 降低温度防止NH4HCO3和FeSO4分解
B. 沉淀过程中有CO2气体放出
C. 过滤操作的常用玻璃仪器有烧杯、漏斗和玻璃棒
D. 产品FeCO3在空气中高温分解可得到纯净的FeO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com