
【题目】标准状况下11.2 L某烃A在一定的条件下,可与1 g H2起加成反应生成通式为CnH2n的直链烃,将加成产物燃烧可得二氧化碳88g。下列可能为烃A名称的是
A.2—甲基丙烷 B.1,3—丁二烯 C.2—甲基丙炔 D.2—甲基丙烯
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】据报道氢氧燃料电池公交汽车已经驶上北京街头,下列说法中正确的是( )
A.氢氧燃料电池把氢气和氧气燃烧放出的热能转化为电能
B.电解水制取氢气是理想而经济的制氢方法
C.氢氧燃料电池汽车的使用可以有效减少城市空气污染
D.燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.离子化合物中可以含有共价键,但共价化合物中一定不含离子键
B.含有共价键的物质一定是共价化合物
C.分子中一定含有化学键
D.含有金属元素的离子一定是阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质能使品红溶液褪色,且褪色原理基本相同的是( )
①活性炭
②氯水
③二氧化硫
④臭氧
⑤过氧化钠
⑥双氧水.
A.①②④
B.②③⑤
C.②④⑤⑥
D.③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示氮及其化合物在一定条件下的转化关系:
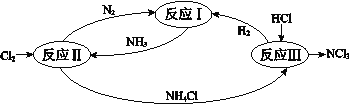
(1)根据反应I,在500℃、20MPa时,将N2和H2通入到体积为2 L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:

(1)10 min内用NH3表示该反应的平均速率,v(NH3)= 。
(2)在10~20min内NH3浓度变化的原因可能是 (填字母)。
a.加了催化剂
b.降低温度
c.增加NH3的物质的量
(3)该可逆反应达到平衡的标志是_______(填字母)。
a.3v(H2)正 = 2v(NH3)逆
b.混合气体的密度不再随时间变化
c.容器内的总压强不再随时间而变化
d. N2、H2、NH3的分子数之比为1∶3∶2
(4)第一次平衡时,平衡常数K1= (用数学表达式表示)。
(5)反应I:N2(g)+3H2(g)![]() 2NH3(g) ΔH=–92.4 kJmol-1
2NH3(g) ΔH=–92.4 kJmol-1
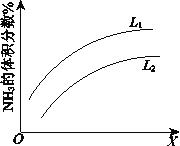
如图所示反应I中平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是____________(填“温度”或“压强”),判断L1、L2的大小关系并说明理由_______ 。
(6)反应II其中一步反应为
2NH3 (g)+3Cl2(g) =N2 (g) +6HCl(g) ΔH=–462 kJmol-1
已知:![]()
断开1 mol H–N键与断开1 mol H–Cl键所需能量相差约为_________ kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A(g)+3B(g)![]() 2C(g)+D(s),1molA和3molB在2L密闭容器中进行上述反应,若2min后,测得C的浓度为0.2mol/L,则下列说法正确的是( )
2C(g)+D(s),1molA和3molB在2L密闭容器中进行上述反应,若2min后,测得C的浓度为0.2mol/L,则下列说法正确的是( )
A.v(D)=0.05mol/(Lmin) B.v(B)=0.15mol/(Lmin)
C. 3v(B)=2v(C) D.A的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有足量A的体积可变的密闭容器中,保持压强一定,加入B,发生反应:A(s)+2B(g) ![]() 4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是( )
4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是( )
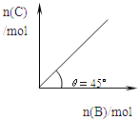
①若当温度升高后,则图中θ>45°
②若再加入B,则正、逆反应速率均逐渐增大
③若再加入B,则再次达到平衡时反应体系气体密度不变
④平衡时B的转化率为50%
A.①③ B.②③ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中能大量共存的是( )
A.Al3+、NO3﹣、OH﹣、Cl﹣
B.H+、Ba2+、Ag+、Cl﹣
C.Fe2+、Fe3+、Na+、NO3﹣
D.Ca2+、H+、Cl﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下将0.1mol N2和0.3mol H2置于恒容密闭容器中发生反应:N2+3H2![]() 2NH3.下列关于该反应的说法正确的是( )
2NH3.下列关于该反应的说法正确的是( )
A.最终可生成0.2 mol NH3
B.增大压强能使反应速率减小
C.降低反应体系的温度能加快反应速率
D.向容器中再加入N2,能加快反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com