
【题目】某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。
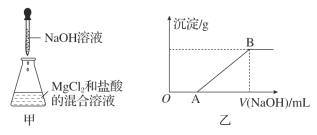
请回答下列问题。
(1)溶解MgCl2固体所用的玻璃仪器有________ (填字母)。
a. 天平 b. 烧杯 c. 漏斗 d. 玻璃棒
(2)OA段反应的化学方程式为_____________________________________。
(3)AB段反应的化学方程式为________________________________________。
(4)在B点对应的溶液中滴加AgNO3溶液,观察到的现象是______________________,反应的离子方程式为___________________________________________。
【答案】b d NaOH + HCl = NaCl + H2O MgCl2 + 2NaOH = Mg(OH)2↓+ 2NaCl 有白色沉淀生成 Ag++Cl-=AgCl↓
【解析】
氯化镁和盐酸的混合溶液中滴入氢氧化钠,首先发生酸碱中和反应:NaOH+HCl═NaCl+H2O,盐酸反应完毕,再发生反应2NaOH+MgCl2=2NaCl+Mg(OH)2↓,
(1)根据固体物质溶解的方法选用仪器;
(2)OA段氢氧化钠与氯化氢反应生成氯化钠和水,据此写出反应的化学方程式;
(3)AB段氯化镁与氢氧化钠反应生成氢氧化镁和氯化钠,据此写出反应的化学方程式;
(4)B点溶液中的溶质为氯化钠,氯化钠与硝酸银溶液反应生成氯化银沉淀。
氯化镁和盐酸的混合溶液中滴入氢氧化钠,首先发生酸碱中和反应:NaOH+HCl═NaCl+H2O,盐酸反应完毕,再发生反应2NaOH+MgCl2=2NaCl+Mg(OH)2↓,
(1)溶解MgCl2固体,应该在烧杯中进行,并用玻璃棒不断搅拌;
故答案为:bd;
(2)OA段:NaOH与氯化氢反应生成氯化钠和水,反应的化学方程式为:NaOH + HCl = NaCl + H2O;
故答案为:NaOH + HCl = NaCl + H2O;
(3)AB段:MgCl2与NaOH反应生成氢氧化镁沉淀,反应的化学方程式为:MgCl2 + 2NaOH = Mg(OH)2↓+ 2NaCl;
故答案为:MgCl2 + 2NaOH = Mg(OH)2↓+ 2NaCl;
(4)根据以上分析B点时镁离子恰好完全沉淀,溶液只剩NaCl,所以滴加AgNO3溶液,观察到的现象为有白色沉淀生成,反应的离子方程式为:Ag++Cl-=AgCl↓;
故答案为:有白色沉淀生成;Ag++Cl-=AgCl↓。


科目:高中化学 来源: 题型:
【题目】有KOH和Ca(OH)2的混合溶液,c(OH﹣)=0.1 molL﹣1。取此溶液500 mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示。图中(V1)为112 mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )
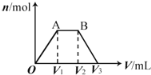
A. 560、672 B. 1008、1120 C. 2240、2352 D. 392、504
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将0.1molL﹣1 NaOH溶液加入20mL0.1molL﹣1CH3COOH溶液中,所加入溶液的体积(V)和混合液的pH关系曲线如图所示。下列结论正确的是( )
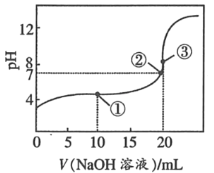
A.①点时,c(CH3COO﹣)+c(CH3COOH)=c(Na+)
B.对曲线上①②③任何一点,溶液中都有c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣)
C.③点时,醋酸恰好完全反应完溶液中有c(CH3COO﹣)=c(Na+)>c(H+)=c(OH﹣)
D.滴定过程中可能出现c(H+)>c(Na+)>c(CH3COO﹣)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁能形成多种化合物,如Fe(SCN)3,[Fe(CO)5](羰基铁),它们在生活生产中有广泛应用。
(1)Fe3+基态核外电子排布式为_____。
(2)实验室用KSCN溶液、苯酚溶液检验Fe3+.N、O、S的第一电离能由大到小的顺序为____ 。SCN﹣中的碳原子的杂化轨道类型为_____。与SCN﹣互为等电子体的分子是_____。
(3)羰基铁[Fe(CO)5]可用作催化剂。1mol[Fe(CO)5]分子中含σ键数目为_____。
(4)某种氮化铁晶胞的晶体如图所示,该氮化铁晶体的化学式为_____。
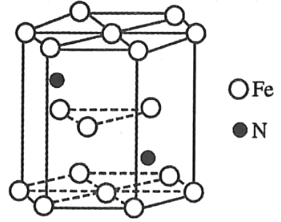
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KCl样品中含有少量KOH、K2SO4和不溶于水的杂质,为了提纯KCl,某同学先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作
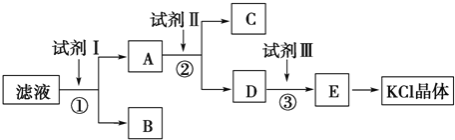
(1)试剂Ⅰ的化学式为__________,其作用是除去__________(填离子符号),
检验该离子完全除尽的操作是__________________________________________
(2)加入试剂Ⅱ时发生反应的化学方程式为_____________________________
(3)试剂Ⅲ的名称是__________,各步操作中所加试剂都必须过量,欲检验试剂Ⅲ已经过量,可以选用__________(填字母).
A.AgNO3 B.pH试纸 C.K2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2俗名称作光气,是有毒气体。在一定条件下,可发生的化学反应为:COCl2(g) ![]() CO(g)+Cl2(g) ΔH<0 下列有关说法不正确的是
CO(g)+Cl2(g) ΔH<0 下列有关说法不正确的是
A. 在一定条件下,使用催化剂能加快反应速率
B. 当反应达平衡时,恒温恒压条件下通入Ar,COCl2的转化率不变
C. 单位时间内生成CO和消耗Cl2的物质的量比为1∶1时,反应达到平衡状态
D. 平衡时,其他条件不变,升高温度可使该反应的平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同物质的量的钠、镁、铝与足量盐酸反应时放出氢气的体积比为__________。分别为0.3 mol的钠、镁、铝投入100 mL 1 mol·L-1的硫酸溶液中,三者产生的体积比是_______。
(2)在一个用铝制的易拉罐内充满CO2气体,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口。经过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起来。罐壁内凹而瘪的原因是_____________,离子方程式可能为____________________;罐再鼓起的原因是________________,离子方程式可能为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
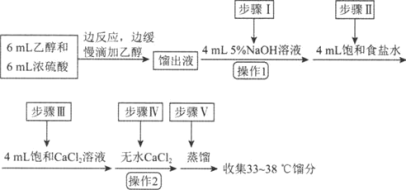
【题目】乙醚是有机合成中常用的溶剂。某实验小组在实验室利用乙醇脱水制备乙醚,装置示意图(夹持和加热装置已略去)、有关数据和实验步骤如下:
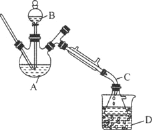
物质 | 相对分子质量 | 密度/(g·mL-1) | 沸点/℃ | 在水中的溶解性 |
乙醇 | 46 | 0.816 | 78 | 互溶 |
乙醚 | 74 | 0.713 | 34.6 | 不溶 |
已知:①相同条件下,乙醚在饱和食盐水中比在水中更难溶。
②氯化钙可与乙醇形成络合物CaCl2·6C2H5OH。
请回答下列问题:
(1)仪器B的名称为________。
(2)由乙醇制备乙醚的总反应为2C2H5OH![]() CH3CH2OCH2CH3+H2O,此反应分两步进行,第一步反应的化学方程式为:CH3CH2OH+H2SO4
CH3CH2OCH2CH3+H2O,此反应分两步进行,第一步反应的化学方程式为:CH3CH2OH+H2SO4![]() CH3CH2OSO2OH+H2O,则第二步反应的化学方程式为________。
CH3CH2OSO2OH+H2O,则第二步反应的化学方程式为________。
(3)反应过程中,仪器B的末端应浸入反应液中,原因是________________。
(4)仪器D中盛有冰水混合物,其作用为________________。
(5)操作1的名称为________,操作2的名称为________。
(6)若省略步骤Ⅱ会导致的后果是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示甲是某学生验证铜和浓硝酸反应的装置,乙、丙是另外两位同学对甲装置改进后的装置:
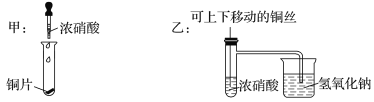
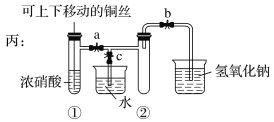
(1)甲、乙、丙三个装置中共同发生的反应的化学方程式是__________________________________。
(2)和甲装置相比,乙装置的优点是①______________________;②________________。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭活塞________,再打开活塞________,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应该_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com