
【题目】下列转化过程中必须加入还原剂的是
A. Cl2→Cl- B. SO2→SO32- C. Fe3+→Fe2+ D. Cu→Cu2+
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,反应2SO2+ O2![]() 2SO3,达到平衡时,n(SO2):n(O2):n(SO3)= 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是
2SO3,达到平衡时,n(SO2):n(O2):n(SO3)= 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是
A. 0.4mol B. 0.6mol C. 0.8mol D. 1.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,其原子序数依次增大,在周期表中A的原子半径最小,B的主族序数是周期序数的2倍,D是地壳中含量最多的元素,在周期表中A和E同主族,回答下列问题:
(1)化合物BD2的电子式是_______。
(2)化合物CA3的结构式为______。
(3)C的最低价氢化物与C的最高价氧化物的水化物反应生成盐的化学式为____。
(4)用电子式表示化合物A2D的形成过程:____________。
(5)将物质的量比为1:1的CO2和H2O组成的混合气通入到a mol的过量固体E2D2中,将反应后的固体混合物加入到500mL1mol·L-1盐酸中,则产生无色混合气体的体积在标准状况下为bL,反应后溶液呈中性,则a=____,b=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2(g)+3H2(g)![]() 2NH3(g) △H<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
2NH3(g) △H<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
A. 容器内的温度不再变化
B. 容器内的压强不再变化
C. 相同时间内,断开H-H键的数目和生成N-H键的数目相等
D. 容器内气体的浓度c(N2):c(H2):c(NH3)=1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下的定容密闭容器中,发生反应2SO2(g)+ O2(g) ![]() 2SO3(g), 下列哪种情况,能表明反应达到平衡状态
2SO3(g), 下列哪种情况,能表明反应达到平衡状态
A. SO2速率是O2速率的2倍
B. SO3的浓度是O2浓度的2倍
C. SO3的质量分数保持不变
D. 单位时间内SO2消耗的浓度等于SO3生成的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向圆底烧瓶中加入1 molC2H5OH和含1molHBr的氢溴酸,溶液中发生反应;C2H5OH+HBr![]() C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是
C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是
A. 加入NaOH,可增大乙醇的物质的量
B. 增大HBr浓度,有利于生成C2H5Br
C. 若反应物增大至2 mol,则两种反应物平衡转化率之比不变
D. 若起始温度提高至60℃,可缩短反应达到平衡的时间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 氧气和臭氧互为同素异形体
B. CH3CH2OH和CH3OCH3互为同分异构体
C. ![]() 和
和![]() 互为同位素
互为同位素
D. ![]() 的最外层电子数为2,所以
的最外层电子数为2,所以![]() 具有较强的金属性
具有较强的金属性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选择下列化学用语,用序号完成下列问题①O2②Na2O2③18O④CH3—CH2—CH2—CH2—CH3⑤O2-⑥CaCl2 ⑦O3 ⑧16O ⑨NH4Cl ⑩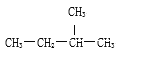
(1)只含共价键的是___________________。
(2)既含共价键又含离子键的是___________________。
(3)属于离子晶体的是______________,属于共价化合物的是_________________。
(4)互为同素异形体的是______,互为同分异构体的是______,互为同位素的是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组混合液:①汽油和水;②75%的酒精溶液;③碘的水溶液,分离以上各混合液的正确方法依次是
A. 分液、萃取、蒸馏 B. 分液、蒸馏、萃取
C. 萃取、蒸馏、分液 D. 蒸馏、萃取、分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com