

| A. | 电子方向:Zn→Cu | |
| B. | Cu电极逐渐溶解 | |
| C. | Zn电极上发生还原反应 | |
| D. | 盐桥中装有含氯化钾的琼脂,Cl-向右池移动 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
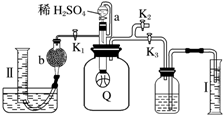 为了测定已部分变质的过氧化钠样品的纯度,设计如图所示的实验装置,图中Q为弹性良好的气球(不与药品反应),称取一定量的样品放入其中.按如图所示的装置安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中.
为了测定已部分变质的过氧化钠样品的纯度,设计如图所示的实验装置,图中Q为弹性良好的气球(不与药品反应),称取一定量的样品放入其中.按如图所示的装置安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种微粒所含有的电子数相等 | B. | 三种微粒中氮原子的杂化方式相同 | ||
| C. | 三种微粒的空间构型相同 | D. | 键角大小关系:NH4+>NH3>NH2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| B. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA | |
| C. | 1.0L的0.1 mol•L-1Na2S溶液中含有的S2-离子数为0.1NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
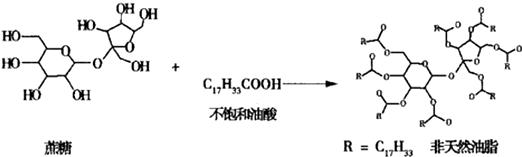
| A. | 该非天然油脂与氢氧化钠溶液共热,产物可与溴的四氯化碳溶液反应 | |
| B. | 天然油脂、蔗糖、非天然油脂都能发生水解反应 | |
| C. | 蔗糖、葡萄糖分别与银氨溶液水浴加热反应,有相同的实验现象 | |
| D. | 植物油、非天然油脂都可以与H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
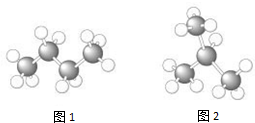
| A. | 图1表示的烃叫丙烷 | |
| B. | 图2烃分子的结构简式为CH3CH2CH2CH3 | |
| C. | 图1与图2表示的是同一种物质 | |
| D. | 图1与图2表示的物质互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{a}^{b}$R | B. | ${\;}_{a}^{a+b}$R | C. | ${\;}_{a-m}^{a+b-m}$R | D. | ${\;}_{a+m}^{a+b+m}$R |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com