
 MnCl2+Cl2↑+2H2O中,如转移电子的物质的量是4mol,则被氧化的HCl的物质的量是______mol,有______ mol Cl2生成.
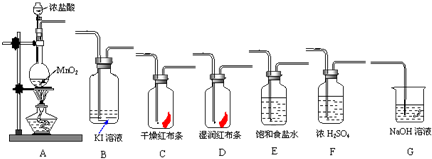
MnCl2+Cl2↑+2H2O中,如转移电子的物质的量是4mol,则被氧化的HCl的物质的量是______mol,有______ mol Cl2生成.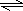 H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl;氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使有色布条褪色,所以看到的现象是湿润的红色布条褪色;氯气能和碘化钾发生置换反应生成碘单质,所以看到的现象是溶液由无色变为褐色,
H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl;氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使有色布条褪色,所以看到的现象是湿润的红色布条褪色;氯气能和碘化钾发生置换反应生成碘单质,所以看到的现象是溶液由无色变为褐色, Mn 2++Cl2↑+2H2O;
Mn 2++Cl2↑+2H2O; Mn 2++Cl2↑+2H2O;2I-+Cl2=I2+2Cl-;Cl2+2OH-=Cl-+ClO-+H2O;
Mn 2++Cl2↑+2H2O;2I-+Cl2=I2+2Cl-;Cl2+2OH-=Cl-+ClO-+H2O; MnCl2+Cl2↑+2H2O 转移电子
MnCl2+Cl2↑+2H2O 转移电子

科目:高中化学 来源: 题型:

| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:
MnO2+4HCl(浓) Cl2↑+MnCl2+2H2O
试回答下列问题:
(1)该反应是氧化还原反应吗?① (填“是”或“不是”),如果是氧化还原反应,指出②氧化剂是 ,③还原剂是 ,④写出该反应的离子方程式 。
(2)集气瓶A中盛装的是饱和食盐水(注:氯气在饱和食盐水中溶解度很小,而氯
化氢在饱和食盐水中的溶解度则很大),其作用是 。
(3)氯气溶于水显酸性,且氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中
毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用 溶液来吸收有毒的氯气。
(4)一次实验中,加入浓盐酸200mL,其密度为1.19g·cm-3、HCl的质量分数为36.5%,
当MnO2刚好完全反应时,产生了5.6L(标准状况)的氯气。
试计算该浓盐酸的物质的量浓度和被氧化的HCl的物质的量。(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2015届山西省高一上学期期末联考化学试卷(A)(解析版) 题型:计算题
(共12分)实验室里通常用MnO2与浓盐酸在加热的条件下反应制取氯气,为进行有关氯气的性质实验,需要4瓶容积为100ml的氯气(标准状况)。
(1)写出实验室制取氯气的化学反应方程式并标出电子转移的方向及数目。
(2)制取4瓶氯气,理论上需要MnO2固体的质量是多少?(浓盐酸过量,并可以补充)
(3)实际称量的MnO2固体的质量必需多于理论量,主要原因是什么?
查看答案和解析>>
科目:高中化学 来源:2013届辽宁省锦州市高一上学期期末考试化学试卷 题型:实验题
实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:
MnO2+4HCl(浓) Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
试回答下列问题:
(1)该反应是氧化还原反应吗?① (填“是”或“不是”),如果是氧化还原反应,指出②氧化剂是 ,③还原剂是 ,④写出该反应的离子方程式 。
(2)集气瓶A中盛装的是饱和食盐水(注:氯气在饱和食盐水中溶解度很小,而氯
化氢在饱和食盐水中的溶解度则很大),其作用是 。
(3)氯气溶于水显酸性,且氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中
毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用 溶液来吸收有毒的氯气。
(4)一次实验中,加入浓盐酸200mL,其密度为1.19g·cm-3、HCl的质量分数为36.5%,
当MnO2刚好完全反应时,产生了5.6L(标准状况)的氯气。
试计算该浓盐酸的物质的量浓度和被氧化的HCl的物质的量。(请写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com