
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
分析 Ⅰ.(1)二氧化锰是过氧化氢分解的催化剂,由带火星木条复燃,可知产物,由此可写出方程式;
(2)由实验现象可知催化剂作用大小的影响因素;
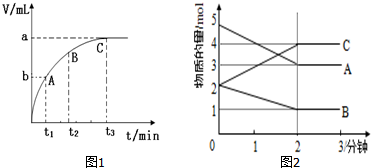
(3)A、B、C三点的斜率代表反应速率,斜率越大,反应速率越大;
Ⅱ.(4)从物质的物质的量的变化趋势判断反应物和生成物,根据物质的物质的量变化值等于化学计量数之比书写化学方程;
(5)化学反应速率是单位时间内浓度的变化,据此可求得反应速率;
(6)可逆反应达到平衡状态时,正逆反应速率相等,各组分浓度不再变化,若存在有色物质,则有色物质的颜色也不再变化,据此对各选项进行判断;
(7)根据$\frac{平衡时A的物质的量}{平衡时气体总物质的量}$,可求得平衡时A的体积分数.
解答 解:(1)上述实验中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)时间少,则反应速率快,则实验结果表明,催化剂的催化效果与催化剂的表面积有关,
故答案为:催化剂的表面积;
(3)由图可知,曲线斜率变小,反应速率减小,则A、B、C三点所表示的反应速率最慢的是C,
故答案为:C;
Ⅱ.(4)由图象可以看出,A、B的物质的量逐渐减小,则A、B为反应物,C的物质的量逐渐增多,所以C为生成物,当反应到达2min时,△n(A)=2mol,△n(B)=1mol,△n(C)=2mol,化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(A):△n(B):△n(C)=2:1:2,所以反应的化学方程式为:2A+B?2C,
故答案为:2A+B?2C;
(5)由图象可以看出,反应开始至2分钟时,△n(B)=1mol,B的平均反应速率为:$\frac{1mol}{5L}$÷2min=0.1mol/(L•min),
故答案为:0.1mol/(L•min);
(6)a.v(A)=2v(B)不能说明正反应和逆反应的关系,故无法判断反应是否达到平衡,故a错误;
b.容器内各物质的物质的量相等,不能说明各组分的浓度不再变化,无法判断是否达到平衡状态,故b错误;
c.在该反应中A和C的计量数相等,当v逆(A)=v正(C)时,正逆反应速率相等,说明反应已达平衡状态了,故c正确;
d.只有A为有色物质,当容器内气体的颜色保持不变,说明各组分的浓度不再变化,该反应已经达到平衡状态,故d正确;
故答案为:cd;
(7)由图象可知:达平衡时A的物质的量为3mol,平衡时总物质的量为1mol+3mol+4mol=8mol,
所以A的体积分数为$\frac{平衡时A的物质的量}{平衡时气体总物质的量}$=$\frac{3mol}{8mol}$×100%=37.5%,
故答案为:37.5%.
点评 本题考查影响化学反应速率因素及化学平衡图象的计算,题目难度中等,注意把握由图象判断化学方程式的方法以及反应现象与结论的推断,试题侧重考查学生的分析能力及化学计算、化学实验能力.


科目:高中化学 来源: 题型:解答题
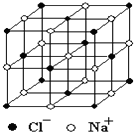 晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl的晶胞如图所示,随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度也越来越高.现有一简单可行的测定方法,具体步骤如下:①将NaCl固体研细、干燥后,准确称取m g NaCl固体并转移到定容仪器A中.②用滴定管向A仪器中加苯,不断振荡,继续加苯到A仪器的刻度线,计算出NaCl固体的体积为V mL.回答下列问题:
晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl的晶胞如图所示,随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度也越来越高.现有一简单可行的测定方法,具体步骤如下:①将NaCl固体研细、干燥后,准确称取m g NaCl固体并转移到定容仪器A中.②用滴定管向A仪器中加苯,不断振荡,继续加苯到A仪器的刻度线,计算出NaCl固体的体积为V mL.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠、镁、铝的还原性依次减弱 | |
| B. | NaOH、Mg(OH)2、Al(OH)3碱性依次增强 | |
| C. | HCl、HBr、HI的稳定性依次增强 | |
| D. | HClO4、H2SO4、H3PO4的酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硝酸 | B. | 溴水 | C. | KSCN溶液 | D. | 酸性高锰酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为90. |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重 5.4g和13.2g. | (2)A的分子式为C3H6O3. |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团 -COOH、-OH |
(4)A的核磁共振氢谱如下图: | (4)A中含有4种氢原子. 综上所述, A的结构简式为  . . |
| (5)两分子A可反应生成一个六元环状化合物 | (5)写出此反应的方程式 2  $→_{△}^{浓硫酸}$ $→_{△}^{浓硫酸}$ +2H2O +2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乳酸薄荷醇酯(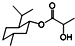 )不仅能发生氧化、消去反应,还能发生取代反应 )不仅能发生氧化、消去反应,还能发生取代反应 | |
| B. | 乙醛和丙烯醛( )不是同系物,它们与氢气充分反应后的产物也不是同系物 )不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| C. | 按系统命名法,化合物 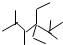 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| D. | 化合物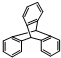 是苯的同系物 是苯的同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com