
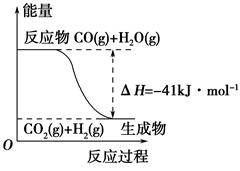

| A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=41 kJ·mol-1 |
| B.该反应为吸热反应 |
| C.该反应为放热反应 |
| D.当H2O为液态时,其反应热值小于41 kJ·mol-1 |

 2NH3(g) ΔH=-92 kJ·mol-1
2NH3(g) ΔH=-92 kJ·mol-1

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
A.NH4Cl NH3↑+HCl↑ NH3↑+HCl↑ |
B.NH3+CO2+H2O NH4HCO3 NH4HCO3 |
C.2NaOH+Cl2 NaCl+NaClO+H2O NaCl+NaClO+H2O |
D.2Na2O2+2CO2 2Na2CO3+O2 2Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ⅠA族元素成键时不可能有杂化轨道 |
| B.杂化轨道既可能形成σ键,也可能形成π键 |
| C.孤对电子有可能参加杂化 |
| D.s轨道和p轨道杂化不可能有sp4出现 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.因为NaHSO4是离子化合物,因此能够导电 |
| B.NaHSO4固体中阳离子和阴离子的个数比是2:1 |
| C.NaHSO4固体熔化时破坏的是离子键和共价键 |
| D.NaHSO4固体溶于水时既破坏离子键又破坏共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有非金属原子间才能形成共价键 |
| B.共价化合物中不可能含有离子键 |
| C.单质中不可能含有离子键 |
| D.非金属单质中不一定含有共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物中一定不含共价键 |
| B.金属元素与非金属元素组成的化合物一定是离子化合物 |
| C.非金属元素组成的化合物一定是共价化合物 |
| D.含有阴离子的化合物一定含有阳离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子键没有方向性和饱和性,而共价键有方向性和饱和性 |
| B.两种不同的非金属元素可以组成离子化合物 |
| C.配位键在形成时,是由成键双方各提供一个电子形成共用电子对 |
| D.金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.变化时有电子的得失或共用电子对的形成 |
| B.变化过程中有化学键的断裂和形成 |
| C.变化时释放出能量 |
| D.变化前后原子的种类和数目没有改变,分子种类增加了 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com