
| A.变化时有电子的得失或共用电子对的形成 |
| B.变化过程中有化学键的断裂和形成 |
| C.变化时释放出能量 |
| D.变化前后原子的种类和数目没有改变,分子种类增加了 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
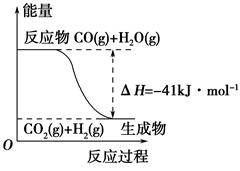

| A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=41 kJ·mol-1 |
| B.该反应为吸热反应 |
| C.该反应为放热反应 |
| D.当H2O为液态时,其反应热值小于41 kJ·mol-1 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | | | |
| X | | | |
| W | Y | | R |
| | | Z | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.共价键的饱和性 |
| B.S原子电子排布 |
| C.共价键的方向性 |
| D.S原子中p轨道的形状和空间伸展方向 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaF | B.MgCl2 | C.NaCl | D.CaCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 |
| B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
| C.已知:①2H2(g)+O2(g)=2H2O(g)ΔH=-a kJ·mol-1, ②2H2(g)+O2(g)=2H2O(l)ΔH=-b kJ·mol-1,则a>b |
| D.已知:①C(s,石墨)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1, |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com