
【题目】铜单质及其化合物在很多领域有重要的用途.
![]() 一
一![]() 如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和
如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和![]() 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
(1)超细铜粉的某制备方法如下:
![]()
![]() 中所含的化学键有 ______ .
中所含的化学键有 ______ .
(2)氯化亚铜![]() 的制备过程是:向
的制备过程是:向![]() 溶液中通入一定量
溶液中通入一定量![]() ,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
![]() 二
二![]() 波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知
波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知![]() 的部分结构可表示如下:
的部分结构可表示如下:

(1)写出铜原子价电子层的电子排布式 ______ ,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有 ______ ![]() 填元素符号
填元素符号![]() .
.
(2)请在上图中把![]() 结构中的化学键用短线“--”表示出来.______
结构中的化学键用短线“--”表示出来.______
(3)往浓![]() 溶液中加入过量较浓的
溶液中加入过量较浓的![]() 直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的
直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的![]() 并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色
并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色![]() 晶体.实验中所加
晶体.实验中所加![]() 的作用是 ______ .
的作用是 ______ .
(4)![]() 晶体中呈正四面体的原子团是 ______ ,杂化轨道类型是
晶体中呈正四面体的原子团是 ______ ,杂化轨道类型是![]() 杂化的原子是 ______ .
杂化的原子是 ______ .
【答案】离子键、共价键和配位键 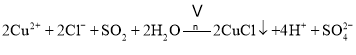
![]() K、Cr
K、Cr ![]() 加
加![]() ,减小“溶剂”
,减小“溶剂”![]() 和
和![]() 的极性,降低离子化合物
的极性,降低离子化合物![]() 的溶解度
的溶解度 ![]() N、S、O
N、S、O
【解析】
(一)根据物质的组成分析化学键的类型;根据氧化还原反应原理书写离子方程式;(二)根据核外电子排布规律分析价层电子排布式;根据物质的极性于溶解性的关系分析解答;根据等电子体理论及价层电子对数分析微粒的空间结构及轨道杂化类型。
(一)(1)![]() 中硫酸根离子和
中硫酸根离子和![]() 存在离子键,N原子和铜原子之间存在配位键,
存在离子键,N原子和铜原子之间存在配位键,![]() 中H和N之间存在共价键,所以
中H和N之间存在共价键,所以![]() 中所含的化学键有共价键、离子键、配位键; 故答案为:共价键、离子键、配位键;
中所含的化学键有共价键、离子键、配位键; 故答案为:共价键、离子键、配位键;
(2)该反应中二氧化硫作还原剂生成硫酸根离子,铜离子得电子生成亚铜离子,反应条件是加热,所以该反应的离子方程式为:![]() ;故答案为:
;故答案为:![]() ;
;
(二)(1)![]() 原子3d、4s能级上电子为其价电子,3d能级上有10个电子、4s能级上有1个电子,其价电子排布式为
原子3d、4s能级上电子为其价电子,3d能级上有10个电子、4s能级上有1个电子,其价电子排布式为![]() ;与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素K、Cr元素, 故答案为:
;与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素K、Cr元素, 故答案为:![]() ;K、Cr;
;K、Cr;
(2)该物质中含有配位键,Cu原子和水分子中O原子之间存在配位键,Cu原子提供空轨道、水分子中O原子提供孤电子对,硫酸根离子中S原子和O原子之间存在共价键,水分子中O原子和H原子之间存在共价键,所以存在的化学键有![]() , 故答案为:
, 故答案为:![]() ;
;
(3)加![]() ,减小“溶剂”
,减小“溶剂”![]() 和
和![]() 的极性,降低离子化合物
的极性,降低离子化合物![]() 的溶解度,有利于
的溶解度,有利于![]() 结晶析出;故答案为:加
结晶析出;故答案为:加![]() ,减小“溶剂”
,减小“溶剂”![]() 和
和![]() 的极性,降低离子化合物
的极性,降低离子化合物![]() 的溶解度;
的溶解度;
(4)![]() 晶体中,
晶体中,![]() 与SiCl4互为等电子体,所以呈正四面体的原子团是
与SiCl4互为等电子体,所以呈正四面体的原子团是![]() ,杂化轨道类型是
,杂化轨道类型是![]() 的原子,其价层电子对个数是4,有N原子、S原子和O原子,故答案为:
的原子,其价层电子对个数是4,有N原子、S原子和O原子,故答案为:![]() ;N、S、O。
;N、S、O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图是三种酸对Fe-Cr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是( )

A.Cr含量小于13%时,因为三种酸中硫酸的氢离子浓度最大,所以对Fe-Cr合金的腐蚀性最强
B.Cr含量等于13%时,三种酸对Fe-Cr合金的腐蚀速率由快到慢的顺序为H2SO4>HCl>HNO3
C.随着Fe含量的增加,Fe-Cr合金在5%HNO3中的耐腐蚀性越来越弱
D.稀硫酸对Fe-Cr合金的腐蚀性比稀硝酸和稀盐酸都强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的恒温恒压密闭容器中投入2molSO3发生反应:2SO3(s) ![]() 2SO2(g)+O2(g) △H= +akJ·mol-1(a>0),2min后达到平衡,此时SO2的物质的量为0.8mol,下列说法正确的是( )
2SO2(g)+O2(g) △H= +akJ·mol-1(a>0),2min后达到平衡,此时SO2的物质的量为0.8mol,下列说法正确的是( )
A.用SO3表示的反应速率为0.2mol·L-1·min-1
B.若O2的体积分数不变,证明该可逆反应已达平衡
C.在2min时,v正(SO2)=2v逆(O2)
D.平衡后,再投入2 mol SO3,则正反应速度加快,逆反应速率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】描述 ![]() 分子结构的下列叙述中,正确的是
分子结构的下列叙述中,正确的是
A.6个碳原子有可能都在一条直线上B.6个碳原子一定都在同一平面上
C.6个碳原子不可能都在同一平面上D.所有原子有可能都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气、汽车尾气排放出的NOx、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
(1)已知:①CO燃烧热的△H1=-283.0kJ·mol-l,②N2(g)+O2(g) ![]() 2NO(g) △H2=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:2NO(g)+2CO(g)
2NO(g) △H2=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g); △H=___。
N2(g)+2CO2(g); △H=___。
(2)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生上述反应,反应过程中部分物质的浓度变化如下图所示.
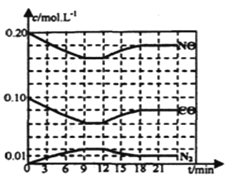
①该反应第一次达到平衡时的平衡常数为________。
②第12min时改变的条件是________。
③在第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将________移动(填“正向”、“逆向”或“不”).
(3)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素。
①SNCR脱硝技术中:在催化剂作用下用NH3作还原剂还原NO,其主要反应为:4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0。体系温度直接影响SNCR技术的脱硝效率,如图所示。当体系温度约为925℃时,SNCR脱硝效率最高,其可能的原因是________。
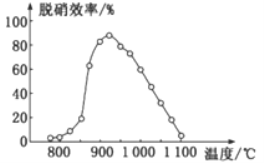
②SCR脱硝技术中则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《hem Commun》报导,MarcelMayorl合成的桥连多环烃(![]() ),拓展了人工合成自然产物的技术。下列有关该烃的说法正确的是( )
),拓展了人工合成自然产物的技术。下列有关该烃的说法正确的是( )
A. 属于饱和烃,常温时为气态B. 二氯代物共有5种
C. 分子中含有4个五元环D. 不存在属于苯的同系物的同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或物质的性质描述正确的是( )
A. 乙烯在一定条件下能发生加成反应,加聚反应,被酸性高锰酸钾溶液氧化
B. 符合分子式为C3H8O的醇有三种不同结构
C. 如图的键线式表示烃的名称为:3-甲基-4-乙基-7-甲基辛烷![]()
D. 治疗疟疾的青蒿素(如图)易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积固定的密闭容器中,达平衡的可逆反应2A(g)![]() 2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
A. B和C可能都是液体 B. B和C肯定都是气体
C. B和C可能都是固体 D. 若C为固体,则B一定是气体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知如下两个热化学反应
![]() (l)+H2(g)→
(l)+H2(g)→![]() (l)
(l)![]() H>0 ①
H>0 ①
![]() (l)+2H2(g)→
(l)+2H2(g)→![]() (l)
(l)![]() H<0 ②
H<0 ②
下列说法不正确的是
A.反应①、②都属于加成反应
B.l,3一环己二烯比苯稳定
C.反应①、②的热效应说明苯环中含有的并不是碳碳双键
D.反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com