
ЁОЬтФПЁПЛЦЬњПѓ(жївЊГЩЗжЮЊFeS2)ЕФгааЇРћгУЖдЛЗОГОпгаживЊвтвхЁЃ
ЃЈ1ЃЉдкЫсадЬѕМўЯТДпЛЏбѕЛЏЛЦЬњПѓЕФЮяжЪзЊЛЏЙиЯЕШчЭМ1ЫљЪОЁЃ
ЂйЭМ1зЊЛЏЙ§ГЬЕФзмЗДгІжа,FeS2зї__________(ЬюЁАДпЛЏМСЁБЁАбѕЛЏМСЁБЛђЁАЛЙдМСЁБЃЌЯТЭЌ)ЁЃИУзЊЛЏЙ§ГЬжаNOЕФзїгУЪЧ________ЁЃ
ЂкаДГіЭМ1жаFe3+гыFeS2ЗДгІЕФРызгЗНГЬЪНЃК________________________ЁЃ


ЃЈ2ЃЉFeS2бѕЛЏЮЊFe3+ЕФЙ§ГЬжа,ПижЦЦ№ЪМЪБFe2+ЕФХЈЖШЁЂШмвКЬхЛ§КЭЭЈШыO2ЕФЫйТЪВЛБфЃЌИФБфЦфЫћЬѕМўЪБ,Fe2+БЛбѕЛЏЕФзЊЛЏТЪЫцЪБМфЕФБфЛЏШчЭМ2ЫљЪОЁЃ
ЂйМгШыNaNO2ЗЂЩњЗДгІЃК2H++3NO2-=NO3-+2NOЁќ+H2OЁЃИУЗДгІжаШєга6molNaNO2ЭъШЋЗДгІ,зЊвЦЕчзгЕФЮяжЪЕФСПЮЊ________molЁЃ
ЂкМгШыNaNO2ЁЂKIЗЂЩњЗДгІЃК4H++2NO2-+2I-=2NOЁќ+I2+2H2OЁЃНтЪЭЭМ2жаИУЬѕМўЯТФмНјвЛВНЬсИпЕЅЮЛЪБМфФкFe2+зЊЛЏТЪЕФдвђЃК__________________ЁЃ
ЁОД№АИЁП ЛЙдМС ДпЛЏМС 14Fe3++FeS2+8H2O==15Fe2++2SO42-+16H+ 4 ЩњГЩЕФДпЛЏМСNOИќЖр,МгПьСЫЗДгІЫйТЪ
ЁОНтЮіЁПЪдЬтЗжЮіЃКЃЈ1ЃЉЂйЭМ1зЊЛЏЙ§ГЬЕФзмЗДгІжаFeS2жаSдЊЫиБЛбѕЛЏЮЊSO42-ЃЛЗДгІЧАКѓNOУЛгаИФБфЃЛЂкИљОнЭМ1ЫљЪОЃЌ Fe3+АбFeS2бѕЛЏЮЊSO42-ЃЌFe3+БЛЛЙдЮЊFe2+ЃЛЃЈ2ЃЉЂйИљОнЕчзгЕчзгзЊвЦЕФЗНЯђКЭЪ§ФП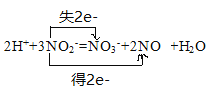 ЗжЮіЃЛЂкNOЪЧИУЗДгІЕФДпЛЏМСЁЃ
ЗжЮіЃЛЂкNOЪЧИУЗДгІЕФДпЛЏМСЁЃ
НтЮіЃКЃЈ1ЃЉЂйЭМ1зЊЛЏЙ§ГЬЕФзмЗДгІжаFeS2жаSдЊЫиБЛбѕЛЏЮЊSO42-ЃЌFeS2ЪЧЛЙдМСЃЛЗДгІЧАКѓNOУЛгаИФБфЃЌЫљвдNOЪЧДпЛЏМСЃЛЂкИљОнЭМ1ЫљЪОЃЌ Fe3+АбFeS2бѕЛЏЮЊSO42-ЃЌFe3+БЛЛЙдЮЊFe2+ЃЛЗДгІРызгЗНГЬЪНЪЧ14Fe3++FeS2+8H2O==15Fe2++2SO42-+16H+ЃЛЃЈ2ЃЉЂйИљОн ЃЌЗДгІжаШєга6molNaNO2ЭъШЋЗДгІ,зЊвЦЕчзгЕФЮяжЪЕФСПЮЊ4molЃЛЂкNOЪЧИУЗДгІЕФДпЛЏМСЃЌМгШыNaNO2ЁЂKIЗЂЩњЗДгІЃК4H++2NO2-+2I-=2NOЁќ+I2+2H2OЃЌЩњГЩЕФДпЛЏМСNOИќЖрЃЌМгПьСЫЗДгІЫйТЪЁЃ
ЃЌЗДгІжаШєга6molNaNO2ЭъШЋЗДгІ,зЊвЦЕчзгЕФЮяжЪЕФСПЮЊ4molЃЛЂкNOЪЧИУЗДгІЕФДпЛЏМСЃЌМгШыNaNO2ЁЂKIЗЂЩњЗДгІЃК4H++2NO2-+2I-=2NOЁќ+I2+2H2OЃЌЩњГЩЕФДпЛЏМСNOИќЖрЃЌМгПьСЫЗДгІЫйТЪЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛУмБеШнЦїжаЃЌГфШывЛЖЈСПЕФЗДгІЮяAЃЌЗДгІ![]() ДяЦНКтКѓЃЌБЃГжЮТЖШВЛБфЃЌНЋШнЦїЬхЛ§ЫѕЕНвЛАыЃЌЕБДяЕНаТЕФЦНКтЪБЃЌBЕФХЈЖШЪЧдРДЕФ1.6БЖЃЌдђ
ДяЦНКтКѓЃЌБЃГжЮТЖШВЛБфЃЌНЋШнЦїЬхЛ§ЫѕЕНвЛАыЃЌЕБДяЕНаТЕФЦНКтЪБЃЌBЕФХЈЖШЪЧдРДЕФ1.6БЖЃЌдђ
A. ЦНКтЯђе§ЗДгІЗНЯђвЦЖЏСЫ B. ЮяжЪAЕФзЊЛЏТЪНЕЕЭ
C. ЮяжЪBЕФжЪСПдіМг D. ![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкЭщЬўаджЪЕФа№ЪіжаЃЌДэЮѓЕФЪЧ( )
A. ЖМФмЪЙЫсадИпУЬЫсМиШмвКЭЪЩЋ
B. ЖМФмШМЩе
C. ЖМВЛШмгкЫЎ
D. ЖМФмЗЂЩњШЁДњЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИјФуЬсЙЉДПаПЦЌЁЂДПЭЦЌКЭ100 mL 0.5 mol/LЕФH2SO4ШмвКЁЂЕМЯпЁЂ1 000 mLСПЭВЁЃЪдгУШчЭМзАжУРДВтЖЈаПКЭЯЁСђЫсЗДгІЪБдкФГЖЮЪБМфФкЭЈЙ§ЕМЯпЕФЕчзгЕФЮяжЪЕФСПЁЃ
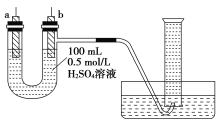
(1)ШчЭМЫљЪОЃЌзАжУЦјУмадСМКУЃЌЧв1 000 mLСПЭВжавбГфТњСЫЫЎЃЌдђПЊЪМЪЕбщЪБЃЌЪзЯШвЊ____________________________ЁЃ
(2)aЕчМЋВФСЯЮЊ________ЃЌЕчМЋЗДгІЪНЮЊ____________________________ЃЛbЕчМЋВФСЯЮЊ________ЃЌЕчМЋЗДгІЪНЮЊ________________________ЁЃ
(3)ЕБСПЭВжаЪеМЏ672 mLЦјЬхЪБ(вбелЫуЕНБъзМзДПіЯТ)ЃЌЭЈЙ§ЕМЯпЕФЕчзгЕФЮяжЪЕФСПЮЊ________ЃЌ________(ЬюЁАaЁБЛђЁАbЁБ)МЋжЪСПМѕЩй________gЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФЦгыЯТСаЮяжЪЗДгІЖМФмЙЛВњЩњЧтЦјЃКЂйH2OЃЛЂкCH3COOHЃЛЂлCH3CH2OHЃЌДгВњЩњЧтЦјЕФОчСвГЬЖШПЩЭЦЖЯГіетШ§жжЮяжЪВњЩњH+ЕФФбвзГЬЖШЪЧЃЈДгФбЕНвзЕФЫГађЃЉЃЈЁЁЁЁЃЉ
A. ЂйЂкЂл B. ЂкЂлЂй C. ЂлЂйЂк D. ЂкЂйЂл
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
A. АзСзКЭКьСзЛЅЮЊЭЌЫивьаЮЬх B. CH3-CH2OHКЭ CH3-O-CH3 ЛЅЮЊЭЌЗжвьЙЙЬх
C. ![]() КЭ
КЭ![]() ЛЅЮЊЭЌЮЛЫи D. ЗжзгМфзїгУСІдНДѓЃЌЗжзгдНЮШЖЈЁЃ
ЛЅЮЊЭЌЮЛЫи D. ЗжзгМфзїгУСІдНДѓЃЌЗжзгдНЮШЖЈЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРћгУЛЏЗЪЩњВњжаЕФЗЯДпЛЏМС(жївЊГЩЗжЮЊAl2O3ЁЂK2OЁЂЩйСПЕФCoOЁЂSiO2ЕШ)РДжЦШЁУїЗЏЕФЙЄвеСїГЬШчЭМЫљЪОЁЃ
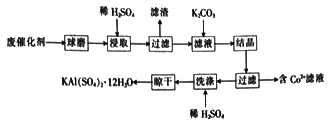
(1)KAl(SO4)2 12H2OжаA1ЕФЛЏКЯМлЮЊ__________ЁЃ
(2)ЗЯДпЛЏМСдкНўШЁЧАНјааЧђФЅЕФжївЊФПЕФЪЧ______________ЁЃ
(3)НўШЁЪБAl2O3ШмНтЕФЛЏбЇЗНГЬЪНЮЊ_________ЃЛТЫдќЕФжївЊГЩЗжЪЧ______________ (ЬюЛЏбЇЪН)ЁЃ
(4)ЪЕбщВтЕУK2CO3ЕФМгШыСПгыKA1(SO4)2 12H2OВњТЪМАДПЖШЙиЯЕШчЯТБэЫљЪОЃК
БрКХ | 1 | 2 | 3 | 4 |
K2CO3МгШыСП/g | 2 | 4 | 6 | 8 |
ВњЦЗжЪСП/g | 3.3 | 5.7 | 4.6 | 4.5 |
УїЗЏДПЖШ/% | 99.1 | 98.2 | 91.4 | 84.9 |
ЕБK2CO3ЕФМгШыСПГЌЙ§4 gКѓЃЌОЇЬхЕФжЪСПМѕЩйЧвДПЖШНЕЕЭЃЌЦфдвђЪЧ__________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзКЭввСНжжЮяжЪЛьКЯЗДгІ(ЗДгІПЩМгШШ)ЃЌНЋЫљЕУЦјЬхЭЈШыЪЪСПЕФБћжаЃЌБћжаУЛгаУїЯдЯжЯѓВњЩњЕФЪЧ (ЁЁЁЁ)
бЁЯю | Мз | вв | Бћ |
A | C | ХЈСђЫс | ГЮЧхЪЏЛвЫЎ |
B | MnO2 | ЯЁбЮЫс | ЦЗКьШмвК |
C | ХЈАБЫЎ | МюЪЏЛв | AlCl3ШмвК |
D | Cu | ХЈЯѕЫс | Ba(HSO3)2ШмвК |
A. A B. B C. C D. D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЭЌбЇРћгУШчЭМЫљЪОзАжУНјааЬњИњЫЎеєЦјЗДгІЕФЪЕбщЃЌВЂМЬајбаОПЬњМАЦфЛЏКЯЮяЕФВПЗжаджЪЁЃ
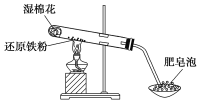
(1)ЪдЙмжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ______________________________________________ЁЃ
(2)ИУЭЌбЇгћШЗЖЈЗДгІвЛЖЮЪБМфКѓЪдЙмжаЙЬЬхЮяжЪЕФГЩЗжЃЌЩшМЦСЫШчЯТЗНАИЃК
ЂйД§ЪдЙмРфШДЃЌШЁЦфжаЙЬЬхЩйаэШмгкЯЁбЮЫсЕУШмвКBЃЛ
ЂкШЁЩйСПШмвКBЕЮМгKSCNШмвКЃЌШєШмвКБфКьЃЌдђЪдЙмжаЙЬЬхЪЧ________(жЛгавЛИібЁЯюЗћКЯЬтвт)ЃЌШєШмвКЮДБфКьЃЌдђЪдЙмжаЙЬЬхЪЧ________(жЛгавЛИібЁЯюЗћКЯЬтвт)ЁЃ
AЃЎвЛЖЈгаFe3O4ЃЌПЩФмгаFe
BЃЎжЛгаFe(OH)3
CЃЎвЛЖЈгаFe3O4КЭFe
DЃЎвЛЖЈгаFe(OH)3ЃЌПЩФмгаFe
EЃЎжЛгаFe3O4
(3)ИУЭЌбЇАДЩЯЪіЗНАИНјааСЫЪЕбщЃЌШмвКЮДБфКьЩЋЃЌдвђЪЧ________________________________(гУЛЏбЇЗНГЬЪНБэЪО)ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com