
����Ŀ����֪E1��134 kJ/mol��E2��368 kJ/mol����ο�����ͼ������Ҫ����գ�
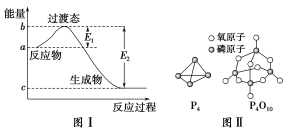
(1)ͼ����1 mol NO2(g)��1 mol CO(g)��Ӧ����CO2(g)��NO(g)�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ���ʼӿ죬E1�ı仯��________(���������С�����䡱����ͬ)����H�ı仯��________��NO2��CO��Ӧ���Ȼ�ѧ����ʽΪ��________________________��
(2)��̼����(��Ҫָ����CO2)�ڽ������������ŷ��о�����Ҫ�����á�ĿǰNH3��(NH4)2CO3�Ѿ���������ҵ��̼����������CO2�ɷ������¿��淴Ӧ��
��Ӧ��2NH3(l)��H2O(l)��CO2(g)![]() (NH4)2CO3(aq) ��H1
(NH4)2CO3(aq) ��H1
��Ӧ��NH3(l)��H2O(l)��CO2(g)![]() NH4HCO3(aq) ��H2
NH4HCO3(aq) ��H2
��Ӧ��(NH4)2CO3(aq)��H2O(l)��CO2(g)![]() 2NH4HCO3(aq) ��H3
2NH4HCO3(aq) ��H3
��H3�릤H1����H2֮��Ĺ�ϵ�ǣ���H3��________��
(3)�±���ʾ�Dz��ֻ�ѧ���ļ��ܲ�����
��ѧ�� | P��P | P��O | O===O | P===O |
����/kJ��mol��1 | a | b | c | x |
��֪����ȼ����Ϊd kJ/mol����������ȫȼ�����ɵIJ���Ľṹ��ͼ����ʾ������x��________ kJ��mol��1(�ú�a��b��c��d�Ĵ���ʽ��ʾ)��
���𰸡�(1)��С ����
NO2(g)��CO(g)===CO2(g)��NO(g) ��H����234 kJ/mol
(2)2��H2����H1
(3) ![]() (d��6a��5c��12b)
(d��6a��5c��12b)
��������(1)��������ܽ��ͷ�Ӧ����Ļ�ܣ���E1��E2����С����E2��E1���䣬����Ӧ�Ȳ��ı䣬��ͼ֪��1 mol NO2��1 mol CO��Ӧ����CO2��NO�ų�����368��134��234 kJ���÷�Ӧ���Ȼ�ѧ����ʽΪNO2(g)��CO(g)===NO(g)��CO2(g) ��H����234 kJ��mol��1��(2)�۲췽��ʽ�����ø�˹���ɣ��ڡ�2���ٵ÷���ʽ�ۣ��ʦ�H3��2��H2����H1��(3)����ȼ�յĻ�ѧ����ʽΪP4��5O2===P4O10��1 mol������ȫȼ�����6 mol P��P��5 mol O===O���γ�12 mol P��O��4 mol P===O����12 mol��b kJ��mol��1��4 mol��x kJ��mol��1��(6 mol��a kJ��mol��1��5 mol��c kJ��mol��1)��d kJ��mol��1�����x��![]() (6a��5c��d��12b) kJ��mol��1��
(6a��5c��d��12b) kJ��mol��1��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ������ȷ�����( )
����� | ������ | ���� | �� | |
A | NaOH��Һ[_K] | ���� | ʯī | ʳ�� |
B | ����ʯ��ˮ | KNO3���� | O3 | ���Na2CO3�� |
C | ���� | ʯ��ʯ | �� | ��ʯ�� |
D | CuSO4��5H2O | CaCl2 | ˮ�� | CaO |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧƽ��һ�������ƶ�����(����)
A. ƽ�������и���ֵ�Ũ�ȷ����ı� B. �����淴Ӧ���ʷ����ı�
C. �����ij���ʵ�ת���ʷ����ı� D. ��ϵ��ѹǿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������л�������A��C2H4 B��![]() C��CH2=CH-CH=CH2 D��HOOCCH2CH2CH2Cl
C��CH2=CH-CH=CH2 D��HOOCCH2CH2CH2Cl
��1��C��Br2�����ʵ���֮��1��1��Ӧ��IJ�����_________��_____________
��2��B�ķ���ʽ��_________
��3�������й�������ȷ����_________
A��C���ܵļӾ۲�����![]()
B��D�еĹ��������Ʒֱ����������ԭ��
C��B��ʹ����KMnO4��Һ��ɫ
D��A���ɵľۺ���������ǡ�CH2-CH2��
��4��D����������Ӧ������Ԫ������
HOOCCH2CH2CH2Cl![]() E
E![]() F
F![]()
![]()
��E�Ľṹ��ʽ_________��F������Ԫ�����Ļ�ѧ����ʽ______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ο�����ͼ������֪E1��134 kJ��mol��1��E2��368 kJ��mol��1������Ҫ��ش��������⣺
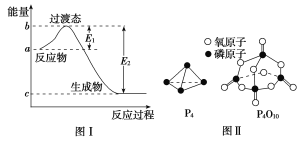
(1)ͼ����1 mol NO2(g)��1 mol CO(g)��Ӧ����CO2��NO�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��________(�������С�����䡱����ͬ)����H�ı仯��__________________________��
��д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��______________________________��
(2)�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧ���Ȼ�ѧ����ʽ���£�
��CH3OH(g)��H2O(g)===CO2(g)��3H2(g)
��H����49.0 kJ��mol��1
��CH3OH(g)��![]() O2(g)===CO2(g)��2H2(g)
O2(g)===CO2(g)��2H2(g)
��H����192.9 kJ��mol��1
��֪��H2O(g)===H2O(l) ��H����44 kJ��mol��1����״�����ȼ��ΪҺ̬ˮ���Ȼ�ѧ����ʽΪ______________________________��
(3)�±���ʾ�Dz��ֻ�ѧ���ļ��ܲ�����
��ѧ�� | P��P | P��O | O===O | P===O |
����/(kJ��mol��1) | a | b | c | x |
��֪����ȼ����Ϊd kJ��mol��1����������ȫȼ�յIJ���Ľṹ��ͼ����ʾ�������x��________kJ��mol��1(�ú�a��b��c��d�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���з��ӻ����������������¶�������KI�������������·�Ӧ��H2O2��H2O��IO3-��I2��MnO4-��Mn2+��HNO2��NO������ֱ��õ����ʵ�������Щ��������������KI,�õ�I2������
A��H2O2 B��IO3- C��MnO4- D��HNO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ԫ�������ڱ��е����λ�����±�����������������Ӧˮ������ǿ��ˮ�ԣ��Ͷ���ͬһ���ڣ���ԭ������������ڲ������ͬ�������������ж���ȷ���ǣ�������

A. �������ԭ���������28
B. ��̬�⻯����ȶ��ԣ�����������
C. �����£��������γɵĻ�����������ˮ
D. ������������ﲻ���κ��ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ�ش�����˵������ȷ����
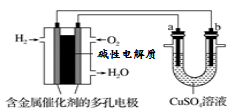
A����װ�����ڵ��ͭʱ�����һ��ʱ�䣬����ͭ��Һ��Ũ�Ȳ���
B����aΪ��ͭ��bΪ��ͭ����װ�ÿ����ڴ�ͭ�ĵ�⾫��
C��ȼ�ϵ����������ӦΪO2��4e����2H2O = 4OH��
D�����Ӿ���������b�缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ�ǵ�����ᷢչ������֧��֮һ,��ר��ָ��:�����ȼ��ȼ�ղ�����CO2��H2O��N2������̫�����������������,ʹ֮�ܹ�ʵ����ͼ��ʾѭ��,��ô������������ȼ�ղ���Դ�������Ⱦ,�����Խ�Լȼ��,������ԴΣ�����ڴ˹��������ѭ����̫��������ת��Ϊ(�� ��)
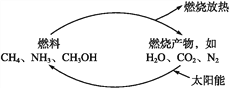
A. ��ѧ�� B. ���� C. �������� D. ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com