
【题目】指出下列原子的杂化轨道类型及分子的结构式、空间构型。
(1)CO2分子中的C采取______杂化,分子的结构式为______,空间构型呈______;
(2)CH2O中的C采取______杂化,分子的结构式为______,空间构型呈______;
(3)H2S分子中的S采取______杂化,分子的结构式为______,空间构型呈______。
【答案】sp O=C=O 直线形 sp2 ![]() 平面三角形 sp3
平面三角形 sp3 ![]() V形
V形
【解析】
根据价层电子对互斥理论确定分子中原子杂化方式及分子空间构型,价层电子对个数=配原子个数+孤电子对个数,据此分析解答。
(1)CO2 分子中C原子的价层电子对数=2+4-2×2=2,2分子的立体构型为直线形,C原子采取sp杂化,在CO2分子中C原子与两个O原子分别形成2对共用电子对,键角是180°,因此该分子是直线型分子,结构式是O=C=O;
(2)CH2O中C原子与2个H原子形成2个σ键,C与O原子形成1个σ键和1个π键,无未成键电子,故中心原子C的杂化轨道数为3,采取sp2杂化,结构式是![]() ,分子的立体构型为平面三角形;
,分子的立体构型为平面三角形;
(3)H2S分子中S原子的价层电子对数是2+![]() =4,VSEPR模型为四面体形,S原子采取sp3杂化分子的立体构型为V形。
=4,VSEPR模型为四面体形,S原子采取sp3杂化分子的立体构型为V形。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图,其中T所处的周期序数与主族序数相等,下列叙述正确的是( )
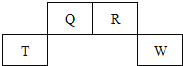
A.离子半径:Tm+>Wn-
B.非金属性:Q>W
C.R的简单氢化物的水溶液呈碱性
D.Q的氧化物都是酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下铁可以和 CO2 发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 CO2 气体,反应过程中 CO2 气体和 CO 气体的浓度与时间的关系如图所示:

(1)t1 时,正、逆反应速率的大小关系为 v 正_____v 逆(填“>”“<”或“=”)。
(2)4 min 内,CO 的平均反应速率 v(CO)=_____。
(3)下列条件的改变能减慢其反应速率的是_____(填序号,下同)。
①降低温度
②减少铁粉的质量
③保持压强不变,充入 He 使容器的体积增大
④保持容积不变,充入 He 使体系压强增大
(4)下列描述能说明上述反应已达平衡状态的是_____。
①v(CO2)=v(CO)
②单位时间内生成 n mol CO2 的同时生成 n mol CO
③容器中气体压强不随时间变化而变化
④容器中气体的平均相对分子质量不随时间变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表的一部分,根据A~I在周期表中的位置,回答以下问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | J | F | H | I |
(1)表中元素,化学性质最不活泼的是___________(用元素符号表示,本小题下同);除稀有气体外,原子半径最大的是___________,可用于制半导体材料的元素是_______;形成化合物中种类最多的元素是___________。
(2)最高价氧化物的水化物酸性最强的是___________(填化学式),A分别与D、E、F、G、H形成的化合物中,最稳定的是___________(填化学式)
(3)元素E和元素H的氢化物均极易溶于水,用两根玻璃棒分别醮取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式___________
(4)B、C两元素的最高价氧化物对应水化物之间反应的离子方程式是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年冬季,我国北方大部分地区出现严重雾霾天气,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等。城市雾霾中还含有铜等重金属元素。
(1)N元素原子核外电子云的形状有___________种;基态铜原子的价电子排布式为___________,金属铜的晶体中,铜原子的堆积方式为___________。
(2)N和O中第一电离能较小的元素是___________;SO42-的空间构型___________。
(3)NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为___________。
(4)测定大气中PM2.5浓度的方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,晶胞边长为540pm,则该晶体的密度___________g/cm3(只列式不计算)(1pm=10-10cm)
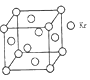
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述合理的是
A. 苯与乙炔的实验式均是C2H2
B. 溴乙烷的比例模型是
C. 羟基的电子式:![]()
D. CH3COOH的电离方程式是CH3COOH=CH3COO-+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图装置完成表中的四个实验,不能达到实验目的的是
实验装置 | 实验目的 | 试剂X | 试剂Y | |
| A. | 检验C2H5Br消去反应后的气体产物 | 水 | 酸性KMnO4溶液 |
B. | 检验C2H5OH消去反应后的气体产物 | NaOH溶液 | Br2的CCl4溶液 | |
C. | 比较醋酸、碳酸、苯酚酸性强弱 | NaOH溶液 | 苯酚钠溶液 | |
D. | 检验制取乙炔时的气体产物 | CuSO4溶液 | 酸性KMnO4溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是基本有机化工原料,由乙炔制各聚乙烯醇和顺式聚异戊二烯的合成路线(部分反应条件略去)如图所示:
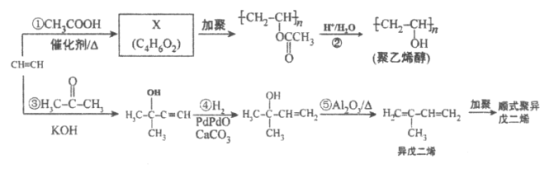
回答下列问题:
(1)按系统命名法命名异戊二烯:__________________________。
(2)写出X加聚的化学反应方程式_____________。
(3)反应①~③中,与反应④的反应类型不同的是_____________(填反应序号)反应⑤属于_____________反应。
(4)与乙炔具有相同官能团的异戊二烯的同分异构体共有_____________种。
(5)X的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是_____(选填字母)。
a. 质谱仪 b. 红外光谱仪 c. 元素分析仪 d. 核磁共振仪
(6)顺式聚异戊二烯的结构式是(选填字母)_____________。
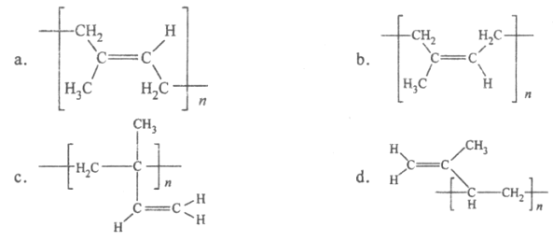
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大。A能分别与B、C、D三种元素形成电子数相同的分子,且B的最外层电子数是次外层电子数的2倍。E的阳离子、D的阴离子均与氖原子的电子层结构相同,且E的单质与D的单质反应能生成E2D和E2D2两种化合物。F所在主族序数与所在周期序数之差为4。(答题时,请用具体的化学用语表示)
(1)元素B在周期表中的位置__________周期________族;C元素的原子结构示意图_________________。
(2)写出由E、F两种元素形成的离子化合物的电子式________________,C2A4的结构式为:_______________,用电子式表示E2D的形成过程:_____________________。
(3)C、D、E形成的简单离子的半径由大到小的顺序为:_____________________。(用离子符号表示)
(4)E的最高价氧化物对应的水化物与F的最高价氧化物对应的水化物之间发生的化学反应方程式为:______________________________________________________________。
(5)向KI溶液中通入适量的F单质后,再滴加一定量的CCl4,振荡静置后的现象为_____________________________________,继续通入F单质并充分振荡,混合溶液逐渐褪为无色,若1mol还原剂转移10NA电子,上述反应的化学方程式为:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com