
����Ŀ����Ȳ�ǻ����л�����ԭ�ϣ�����Ȳ�Ƹ�����ϩ����˳ʽ�������ϩ�ĺϳ�·��(���ַ�Ӧ������ȥ)��ͼ��ʾ��
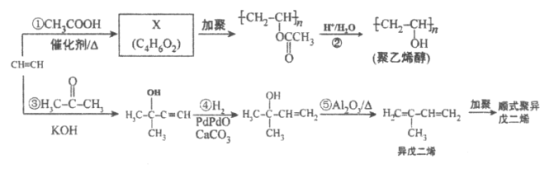
�ش��������⣺
(1)��ϵͳ���������������ϩ��__________________________��
(2)д��X�Ӿ۵Ļ�ѧ��Ӧ����ʽ_____________��
(3)��Ӧ��~���У��뷴Ӧ�ܵķ�Ӧ���Ͳ�ͬ����_____________(�Ӧ���)��Ӧ������_____________��Ӧ��
(4)����Ȳ������ͬ�����ŵ������ϩ��ͬ���칹�干��_____________�֡�
(5)X������ͬ���칹��������һ�ֱ�����������ʾ���ź�(������)��ȫ��ͬ����������_____(ѡ����ĸ)��
a. ������ b. ��������� c. Ԫ�ط����� d. �˴Ź�����
(6)˳ʽ�������ϩ�Ľṹʽ��(ѡ����ĸ)_____________��
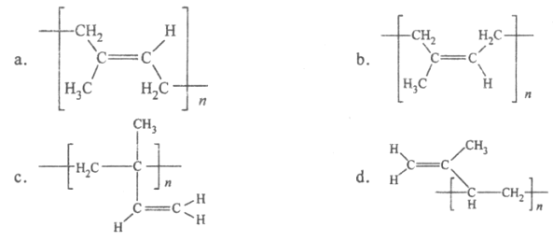
���𰸡�2. ��. 1��3-����ϩ 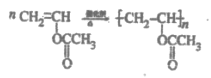 �� ��ȥ��Ӧ 3 c b
�� ��ȥ��Ӧ 3 c b
��������
HC��CH�����ᷢ���ӳɷ�Ӧ����XΪCH2=CHOOCCH3�������Ӿ۷�Ӧ����![]() �� HC��CH���ͪ��KOH�����·�Ӧ����
�� HC��CH���ͪ��KOH�����·�Ӧ����![]() �������������ӳɷ�Ӧ����
�������������ӳɷ�Ӧ����![]() ���������������������������ϩ�������ϩ�ڴ������·����Ӿ۷�Ӧ����˳ʱ�������ϩ
���������������������������ϩ�������ϩ�ڴ������·����Ӿ۷�Ӧ����˳ʱ�������ϩ![]() ���ݴ˷�������
���ݴ˷�������
��1��ѡ��˫�����ڵ�̼��Ϊ����������������4��̼ԭ�ӣ����ʱ̼̼˫�����ȣ��ٱ�֤����λ����С�����Դ���˿�ʼ��ţ�̼̼˫����1��3��λ�Σ�2��̼����1���������������ϩ������2-��-1��3-����ϩ��
��2������X�ļӾ۲���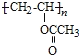 ���ɵ�X�Ľṹ��ʽΪCH2=CHOOCCH3���仯ѧ����ʽΪ��
���ɵ�X�Ľṹ��ʽΪCH2=CHOOCCH3���仯ѧ����ʽΪ��
��3����Ӧ��ΪHC��CH + CH3COOH��CH2=CHOOCCH3�������Ȳ��C2H2�������ᣨC2H4O2���ķ���ʽ��֪�÷�ӦΪ�ӳɷ�Ӧ����Ӧ��Ϊ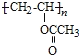 ��
��![]() ������ˮ�������ǻ������Ը÷�ӦΪˮ�ⷴӦ��ȡ����Ӧ����Ӧ��ΪHC��CH���ͪ��KOH�����·�Ӧ����
������ˮ�������ǻ������Ը÷�ӦΪˮ�ⷴӦ��ȡ����Ӧ����Ӧ��ΪHC��CH���ͪ��KOH�����·�Ӧ����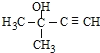 ��������Ȳ���ͪ�ķ���ʽ����֪�÷�ӦΪ�ӳɷ�Ӧ����Ӧ�ܣ�̼̼����ת��Ϊ̼̼˫�����÷�ӦΪ�ӳɷ�Ӧ����Ӧ��Ϊ���ǻ�����ȥ��Ӧ�����Է�Ӧ��~���У���Ӧ�ڵķ�Ӧ�����뷴Ӧ�ܲ�ͬ���ʴ�Ϊ���ڣ���ȥ��Ӧ��
��������Ȳ���ͪ�ķ���ʽ����֪�÷�ӦΪ�ӳɷ�Ӧ����Ӧ�ܣ�̼̼����ת��Ϊ̼̼˫�����÷�ӦΪ�ӳɷ�Ӧ����Ӧ��Ϊ���ǻ�����ȥ��Ӧ�����Է�Ӧ��~���У���Ӧ�ڵķ�Ӧ�����뷴Ӧ�ܲ�ͬ���ʴ�Ϊ���ڣ���ȥ��Ӧ��
��4������Ȳ������ͬ�����ŵ������ϩ������ͬ���칹��Ӧ����C��C�������ܵĽṹ��ʽ��CH3CH(CH3)��C��CH��CH3CH2CH2C��CH��CH3CH2C��CCH3����3�֣��ʴ�Ϊ��3��
��5��a. �������ø��ܵ�����������ӣ�ʹ����ʧȥ���ӱ�Ϊ������ɵķ��ӡ����Ӻ���Ƭ���ӣ�ͬ���칹��õ�����Ƭ��ͬ������������ʾ�����ݲ���ȫ��ͬ��a�����
b. ����������Dzⶨ�ṹ�ģ�ͬ���칹��Ľṹ��ͬ�������������ʾ�����ݲ���ͬ��b�����
c. Ԫ�ط������DzⶨԪ������ģ����ͬ���칹����ʾ��������ȫ��ͬ��c����ȷ��
d. �˴Ź������Dzⶨ��ԭ������ģ��ṹ��ͬ������ԭ�������ȫ��ͬ�����Ժ˴Ź�������ͼ����ȫ��ͬ��d�����
�ʴ�ѡc��
��6��������ͬ��ԭ�ӻ������˫��ͬһ��Ϊ˳ʽ�ṹ������˳ʽ�������ϩ�Ľṹʽ�ǣ�b��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��W��N��ԭ��������������X��ԭ����Ԫ�����ڱ���ԭ�Ӱ뾶��С��Y�Ĵ����������������������![]() �����ӻ�����ZX2��һ�ִ�����ϣ�W��Y����ͬһ���壬NY2��ҽѧ�ϳ��õ�ˮ��������Ư��������������ȷ���ǣ� ��
�����ӻ�����ZX2��һ�ִ�����ϣ�W��Y����ͬһ���壬NY2��ҽѧ�ϳ��õ�ˮ��������Ư��������������ȷ���ǣ� ��
A.Y��W�ֱ���X�γɵļ���������ȶ��ԣ�X2Y>X2W
B.���Ӱ뾶��С�����˳��ΪY2-<Z2+<N-<W2-
C.ZX2��NY2�л�ѧ��һ�£���������֮�Ⱦ�Ϊ1��2
D.����������ԣ�N>W����֤���ǽ����ԣ�N>W
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ָ������ԭ�ӵ��ӻ�������ͼ����ӵĽṹʽ���ռ乹�͡�
(1)CO2�����е�C��ȡ______�ӻ������ӵĽṹʽΪ______���ռ乹�ͳ�______��
(2)CH2O�е�C��ȡ______�ӻ������ӵĽṹʽΪ______���ռ乹�ͳ�______��
(3)H2S�����е�S��ȡ______�ӻ������ӵĽṹʽΪ______���ռ乹�ͳ�______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ǻϳ������ص�ԭ�ϣ����������ȩ�ϳɣ�

�����й�������ȷ����
A. ���ȩ�ķ���ʽ��C8H10O3
B. ���ȩ����NaHCO3��Һ��Ӧ
C. �������ʾ�����������Ȼ�̼��Һ�����ӳɷ�Ӧ
D. ����FeCl3��Һ�������������Ƿ����ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���պ��㴼��������ʳ���㾫����ṹ��ʽ��ͼ��ʾ��
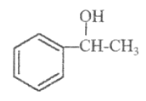
(1)�պ��㴼�ķ���ʽΪ_____________�������ܷ������л���Ӧ������(���������)_____________��
��ȡ����Ӧ �ڼӳɷ�Ӧ ����ȥ��Ӧ �ܼӾ۷�Ӧ ��������Ӧ ��ˮ�ⷴӦ
(2)�л������һ�����ϣ���ϳ�·����ͼ������AΪ������Է�������Ϊ56������Է�������ͨ���������Ϊ88�����ĺ˴Ź���������ʾֻ������壻�����պ��㴼��Ϊͬϵ�
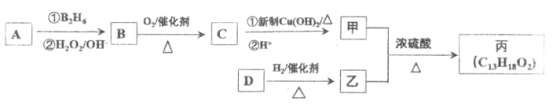
��֪��R-CH=CH2 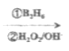 R-CH2CH2OH
R-CH2CH2OH
��A�Ľṹ��ʽ��_____________��
��д����B��C�Ļ�ѧ��Ӧ����ʽ_____________��
��д��C������������ͭ����Һ��Ӧ�Ļ�ѧ��Ӧ����ʽ_____________��
��B��ͬ���칹�������Ʒ�Ӧ�������������ܷ�����������Ӧ����ṹ��ʽ_____________��
�ݱ��к���������CH3��������ҷ�Ӧ�Ļ�ѧ����ʽΪ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�������� CuO �� NH3 ��Ӧ���о� NH3 ��ij�����ʲ��ⶨ����ɣ����������ʵ��װ��(�г�װ��δ����)����ʵ�顣��ش��������⣺
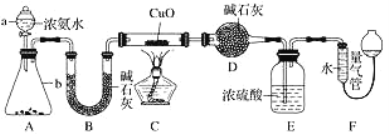
(1)����a������Ϊ_____������b�п�ѡ����Լ�Ϊ________(������)��
(2)ʵ�����У�����װ��A��������ȡ����ɫ������______ (����ĸ)��
A��Cl2 B��O2 C��CO2 D��NO2
(3)ʵ���й۲쵽װ��C�к�ɫCuO��ĩ��Ϊ��ɫ���壬����������ɫ��ζ�����壬��������֤��NH3����______�ԣ�д����Ӧ�Ļ�ѧ����ʽ____________��
(4)Eװ����Ũ���������________��
(5)��ȡ�������ǰ��Ӧ��װ��F���еIJ�����__________��
(6)ʵ����ϣ�����ø����D����mg��װ��F�����������ΪnL(������ɱ�״��)�������е������ԭ�Ӹ�����Ϊ___________(�ú�m��n��ĸ�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.����������Դ�Լ���ˮ��Դ���������ŷdz���Ҫ�����塣
��(1)���������õ�ұ��������____________(�����)��
A.�ȷֽⷨ B.�Ȼ�ԭ�� C.��ⷨ D.ʪ��ұ��
(2)����ұ���õ�����м�ͺ�������ȡ�ĵ������������KI���乤��������ͼ��ʾ��
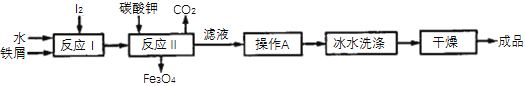
�ٲ���A����________________��_____________�����ˡ�
���ñ�ˮϴ�ӵ�Ŀ���ǣ�a��ȥ������KI����Ŀ��������ʣ�b._________________��
�۷�Ӧ�������������Ļ�����X����X����Ԫ�����Ԫ�ص�������Ϊ21��127����X�Ļ�ѧʽΪ__________________����Ӧ����1molX��ȫ��Ӧ����89.6L(��״��)CO2��д����Ӧ��Ļ�ѧ����ʽ��______________________________________________��
��.��ҵ���ɻ�ͭ��(��Ҫ�ɷ�CuFeS2)ұ��ͭ����Ҫ�������£�

(3)����A�еĴ�����Ⱦ���ѡ�������Լ��е�____________���ա�
a.ŨHSO4 b.ϡHNO3 c.NaOH��Һ d.��ˮ
(4)��ϡH2SO4��������B��ȡ����������Һ���μ�KSCN��Һ��ʺ�ɫ��˵����Һ�д���_____(�����ӷ���)��������Һ�л�����Fe2���ķ����ǣ�____________________________��
(5)��һ�����ľ�ͭ�м���������ϡHNO3��Һ���÷�Ӧ�����ӷ���ʽΪ________________��
(6)����ͭұ����ͭ�Ļ�ѧ��Ӧ����ʽΪ______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ���зdz��ḻ�Ļ�ѧ��Դ���Ӻ�ˮ�п���ȡ���ֻ���ԭ�ϡ�ij�����Ժ�ˮ��Դ�ۺϿ������õIJ��ֹ�������ͼ���¡��ش��������⣺

��1������ʳ��ˮʱ���������У��õ�����______________________�����������
��NaOH��Һ ������ ��K2CO3��Һ ��BaCl2��Һ ������ ��Na2CO3��Һ ��Ba(NO3)2��Һ
��2����ҵ�Ͼ��������������Ʊ�Ba2���������Cl2����Br-Ӧ��________�������Ի���ԣ������½��У������Br2�����ȿ�����������ԭ����_____________________��
��3��Ϊ�˳�ȥ��ҵBr2������Cl2������ҵBr2��____________________��
a.ͨ��HBr b.����Na2CO3��Һ c.����NaBr��Һ d.����Na2SO3��Һ
��4�������������Mg(OH)2�����л���Ca(OH)2���ʣ�д����ȥ���ʵ�ʵ�鲽�� ________________��д��������Լ��Ͳ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪HX�����Ա�HY���������ʵ���Ũ�Ⱦ�Ϊ0.1molL��1��NaX��NaY�����Һ�У�����������ȷ����( )
A. c(OH��)��c(HX)��c(HY)��c(H+)
B. c(OH��)��c(X��)��c(Y��)��c(H+)
C. c(OH��)��c(Y��)��c(X��)��c(H+)
D. c(OH��)��c(HY)��c(HX)��c(H+)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com