
【题目】写出下列反应的化学方程式:
(1)甲酸与新制氢氧化铜悬浊液受热:;
(2)乙二酸和乙二醇酯化成环:;
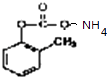
(3)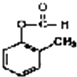 发生银镜反应的化学方程式:;
发生银镜反应的化学方程式:;
(4)丙烯酸甲酯(CH2=CHCOOCH3)加聚反应方程式: .
【答案】
(1)HCOOH+2NaOH+2Cu(OH)2 ![]() Na2CO3+Cu2O↓+4H2O
Na2CO3+Cu2O↓+4H2O
(2)HOCH2CH2OH+HOOCCOOH ![]()
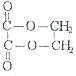 +2H2O
+2H2O
(3)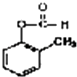 +2Ag(NH3)2OH
+2Ag(NH3)2OH ![]()
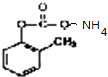 +2Ag↓+3NH3+H2O
+2Ag↓+3NH3+H2O
(4)nCH2=CHCOOCH3 ![]()
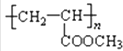
【解析】解:(1)甲酸具有醛的性质,结构简式可以表示为:HO﹣CHO,与新制氢氧化铜悬浊液受热,甲酸中的醛基被氧化,生成碳酸钠,自身被还原成氧化亚铜,反应方程式为:HCOOH+2NaOH+2Cu(OH)2 ![]() Na2CO3+Cu2O↓+4H2O, 所以答案是:HCOOH+2NaOH+2Cu(OH)2
Na2CO3+Cu2O↓+4H2O, 所以答案是:HCOOH+2NaOH+2Cu(OH)2 ![]() Na2CO3+Cu2O↓+4H2O;(2)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯,方程式HOCH2CH2OH+HOOCCOOH
Na2CO3+Cu2O↓+4H2O;(2)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯,方程式HOCH2CH2OH+HOOCCOOH ![]()
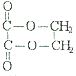 +2H2O;所以答案是:HOCH2CH2OH+HOOCCOOH
+2H2O;所以答案是:HOCH2CH2OH+HOOCCOOH ![]()
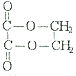 +2H2O;(3)
+2H2O;(3)  可以发生银镜反应生成羧酸铵、金属单质银以及氨气,即
可以发生银镜反应生成羧酸铵、金属单质银以及氨气,即  +2Ag(NH3)2OH
+2Ag(NH3)2OH ![]()
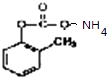 +2Ag↓+3NH3+H2O,所以答案是:
+2Ag↓+3NH3+H2O,所以答案是:  +2Ag(NH3)2OH
+2Ag(NH3)2OH ![]()
 +2Ag↓+3NH3+H2O;(4)丙烯酸甲酯(CH2=CHCOOCH3)含有碳碳双键,发生加聚反应:nCH2=CHCOOCH3
+2Ag↓+3NH3+H2O;(4)丙烯酸甲酯(CH2=CHCOOCH3)含有碳碳双键,发生加聚反应:nCH2=CHCOOCH3 ![]()
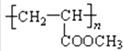 ,所以答案是:nCH2=CHCOOCH3
,所以答案是:nCH2=CHCOOCH3 ![]()
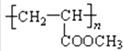 .
.


科目:高中化学 来源: 题型:
【题目】卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多氯代甲烷常为有机溶剂,其分子结构为正四面体的名称为;碳原子个数不大于10的烷烃分子中,其一氯代物只有一种的烷烃的个数为个.
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构式(不考虑立体异构).
(3)聚氯乙烯是生活中常用的塑料,工业生产聚氯乙烯的一种工艺路线如下: 乙烯 ![]() 1,2﹣二氯乙烷
1,2﹣二氯乙烷 ![]() 氯乙烯
氯乙烯 ![]() 聚氯乙烯
聚氯乙烯
反应①的反应类型为;
反应②的反应类型为 .
(4)实验室以乙醇、浓硫酸和溴化钠为试剂,用如图的装置制备溴乙烷,图中省去了加热装置. 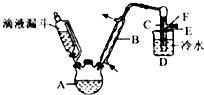
有关数据见表:
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度(g/cm3) | 0.79 | 1.44 | 3.1 |
沸点 | 78.5 | 38.4 | 59 |
①仪器B名称是 , 仪器B的作用是 .
②制备过程中,加入的浓硫酸必须进行稀释,其目的是(填序号)
A.减少副产物烯和醚的生成 B.减少Br2的生成 C.水是反应的催化剂 D.硫酸的浓度越稀反应越快
③加热应采取的方式为;加热的目的是 .
④为除去收集产品中的主要杂质,应选取加入的合理试剂为;采用的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含铬(Cr2O72﹣)废水用硫酸亚铁铵废水用硫酸亚铁铵[FeSO4(NH4)2SO46H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀经干燥后得到n molFeOFeyCrxO3 . 不考虑处理过程中的实际损耗,下列叙述错误的是( )
A.消耗硫酸亚铁铵的物质的量为n(2﹣x)mol
B.处理废水中Cr2O72﹣的物质的量为nx/2mol
C.反应中发生转移的电子数为3nx NA
D.在FeOFeyCrxO3中,3x=y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2 , CO2 , SO2 , NO,CO,不考虑其他成分),设计了如下流程: 
下列说法不正确的是( )
A.固体Ⅰ中主要含有Ca(OH)2、CaCO3、CaSO3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2﹣=N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有相同质量的两份NaHCO3粉末,第一份加入足量盐酸,第二份先加热使其完全分解再加足量同质量分数的盐酸,则两者所消耗的盐酸中氯化氢的质量比为( )
A.2:1
B.1:1
C.1:2
D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含amol氯化铝的溶液中加入bmol氢氧化钾溶液,生成沉淀物质的量可能是( ) ①amol ②bmol ③ ![]() mol ④
mol ④ ![]() mol ⑤0mol ⑥(4a﹣b)mol.
mol ⑤0mol ⑥(4a﹣b)mol.
A.①②④⑤⑥
B.①③⑤
C.①②③⑤⑥
D.①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制备气体和验证气体性质的装置图. 
(1)若利用如图装置制备纯净、干燥的氯气,装置A中反应的化学方程式为 , 装置B盛放;装置C中试剂的作用是 .
(2)若利用如图装置实现碳和浓硫酸的反应,并进行如下验证: ①装置B、C、D、E中分别装有品红溶液、酸性KMnO4溶液、品红溶液、澄清石灰水,则D装置中品红溶液的作用是 , 证明气体中有CO2的现象是 .
②若证明SO2具有氧化性,同时证明碳酸的酸性比硅酸的强,B、C、D中分别装有Na2S溶液、足量酸性KMnO4溶液、品红溶液.
则:B中的现象 , F中应加入溶液,E中发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用生锈的Fe粉和Cu粉的混合物制备CuSO45H2O和FeSO4(NH4)2SO46H2O的工艺流程如图1所示.
已知:①几种物质的溶解度(g/100gH2O)如表所示.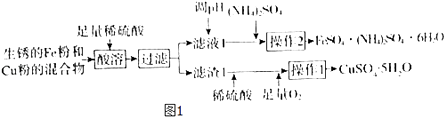
FeSO47H2O | (NH4)2SO4 | FeSO4(NH4)2SO46H2O | |
20℃ | 48 | 75 | 37 |
60℃ | 101 | 88 | 38 |
②溶液pH>4时,Fe2+容易被氧化.
请回答:
(1)过滤所用的主要玻璃仪器为 .
(2)溶液1中的主要溶质为(填化学式).
(3)进行操作2时,从溶液中析出晶体后,需趁热过滤,原因为 .
(4)FeSO4(NH4)2SO46H2O用适量稀硫酸洗涤,而不是用水洗涤的原因为 .
(5)称取2.50gCuSO45H2O样品,灼烧过程中样品质量随温度(T)变化的曲线如图2所示. 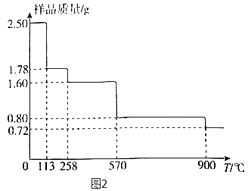
①120℃所的固体,继续加热至258℃时失水,所发生反应的化学方程式为 .
②900℃时剩余固体只有一种铜的氧化物,其化学式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com