
 NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。
NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。 N2H5++N2H3-⑵ N2H4+2HCl=N2H6Cl2 ⑶B(OH)3+H2O
N2H5++N2H3-⑵ N2H4+2HCl=N2H6Cl2 ⑶B(OH)3+H2O [B(OH)4]-+H+ ⑷N2H4(l)+N2O4(l)=N2(g)+H2O(g);△H=-32a KJ/mol。(每空3分)
[B(OH)4]-+H+ ⑷N2H4(l)+N2O4(l)=N2(g)+H2O(g);△H=-32a KJ/mol。(每空3分) N2H5++N2H3-。由于N2H4有两个孤对电子,能与2个H+结合,故1mol N2H4最多能与2molHCl反应。由NH3、N2H4显碱性是因为结合水中的H+,可以推知B(OH)3显酸性应结合水中的OH-,故B(OH)3表现酸性的过程为B(OH)3+H2O
N2H5++N2H3-。由于N2H4有两个孤对电子,能与2个H+结合,故1mol N2H4最多能与2molHCl反应。由NH3、N2H4显碱性是因为结合水中的H+,可以推知B(OH)3显酸性应结合水中的OH-,故B(OH)3表现酸性的过程为B(OH)3+H2O [B(OH)4]-+H+。由题中信息指出“N2H4和N2O4反应产生无污染的气体”可知N在产物中以N2形式存在,进而可知另一物质为H2O。
[B(OH)4]-+H+。由题中信息指出“N2H4和N2O4反应产生无污染的气体”可知N在产物中以N2形式存在,进而可知另一物质为H2O。

科目:高中化学 来源:不详 题型:单选题
| A.C6H12O6(葡萄糖aq)+6O2 ="" 6CO2+6H2O |
| B.CH3COOH+KOH = CH3COOK+H2O |
| C.A+B =C+D;△H<0 |
| D.破坏生成物全部化学键所需能量小于破坏反应物全部化学键所需能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 请回答氯碱的如下问题:
请回答氯碱的如下问题: (1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果);
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果); (2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号)
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号) (3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。 ①
①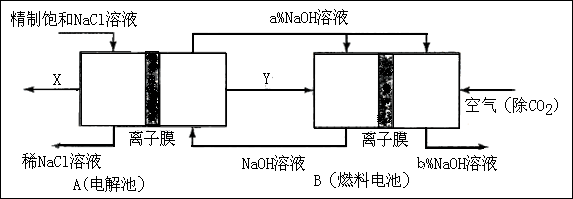 图中X、Y分别是_____、_______(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
图中X、Y分别是_____、_______(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________; ②分别写出燃料电池B中正极、负极上发生的电极反应正极:______; 负极:_____;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______; 负极:_____; ③这样设计的主要节(电)能之处在于(写出2处)____________、____________。
③这样设计的主要节(电)能之处在于(写出2处)____________、____________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH– CO32– SO42– |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物不含共价键 |
| B.共价化合物可能含有离子键 |
| C.离子化合物中只含离子键 |
| D.共价化合物不含离子键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若反应X+Y=M+N是放热反应,该反应一定不用加热 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.原电池正极和负极的材料必须是两种金属 |
| D.铜锌原电池工作时,若有13g锌被溶解,外电路中就有0.4mol电子通过 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com