
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 溶度积/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
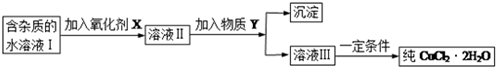
分析 某酸性CuCl2溶液中含有少量的FeCl2,为得到纯净的CuCl2•2H2O晶体,由流程可知,加氧化剂X将亚铁离子氧化为铁离子,X为氯气、氯水、过氧化氢等,但不能引入新杂质,溶液II中加入物质Y为CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3等,促进铁离子的水解生成沉淀,然后过滤得到沉淀为Fe(OH)3,溶液Ⅲ为CuCl2溶液,因水解生成的HCl易挥发,则不能直接加热,应在HCl气流中蒸发结晶得到CuCl2,以此来解答.
解答 解:(1)H2O2作氧化剂的反应产物为水,不会引入新的杂质,所以最适合作氧化剂X的是H2O2;根据表中数据可知Fe3+比Fe2+容易转化为沉淀,因此要把Fe2+转化为Fe3+,所以加入双氧水的目的是将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离;为得到纯净的CuCl2•2H2O晶体,加入的物质来调节pH且不能引进新的杂质,促进铁离子水解转化为沉淀,则加入物质应能转化为氯化铜,则可以加入CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3;
溶液的pH=4,所以溶液中氢离子浓度为10-4 mol/L,则氢氧根离子浓度为10-10 mol/L,c(Fe3+)=$\frac{Ksp[Fe(OH)_{3}]}{{c}^{3}(O{H}^{-})}$=$\frac{4.0×1{0}^{-38}}{(1{{0}^{-10}}_{\;})^{3}}$=4.0×10-8mol/L;
故答案为:C;将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离;CuO(或Cu(OH)2、CuCO3、Cu2(OH)2CO3);4.0×10-8mol/L;
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在HCl气氛中蒸发结晶,
故答案为:在HCl气氛中蒸发结晶.
点评 本题考查混合物分离提纯的综合应用,为高频考点,把握物质的性质、流程中的反应及混合物分离方法、实验技能等为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
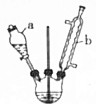 己二酸是合成高分子化合物尼龙-66的原料.某学习小组拟在实验室以环己醇为原料制备己二酸.反应原理如下:
己二酸是合成高分子化合物尼龙-66的原料.某学习小组拟在实验室以环己醇为原料制备己二酸.反应原理如下: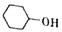 +8HNO3$\stackrel{一定条件}{→}$3HOOC(CH3)4COOH+8NO↑+7H2O
+8HNO3$\stackrel{一定条件}{→}$3HOOC(CH3)4COOH+8NO↑+7H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤燃烧时,化学能主要转化为热能 | |
| B. | 白炽灯工作时,电能转化为光能 | |
| C. | 电解水生成氢气和氧气时,化学能转化为电能 | |
| D. | 绿色植物进行光合作用时,太阳能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
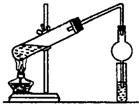 某同学用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图所示.
某同学用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH2CH3 | B. | 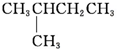 | C. |  | D. | 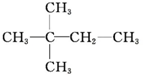 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于5s | B. | 等于10s | C. | 小于10s | D. | 大于10s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com