
����Ŀ���Ȼ������ճ�����ı���Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϣ����γ���NaCl�⣬����������MgCl2��CaCl2��Na2SO4�Լ���ɳ�����ʣ������Ǵ����ᴿ�IJ������̣�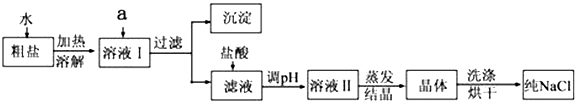
�ṩ���Լ���Na2CO3��Һ��K2CO3��Һ��NaOH��Һ��BaCl2��Һ��Ba��NO3��2��Һ������NaCl��Һ��ϡ���ᣮ
��1������ȥ��ҺI�е�MgCl2��CaCl2��Na2SO4 �� ���ṩ���Լ���ѡ��a���������Լ����Լ���ѡ��͵μ�˳�����ȷ���ǣ���
A.Na2CO3��Һ��BaCl2��Һ��NaOH��Һ
B.��Һ��NaOH��Һ��K2CO3��Һ
C.NaOH��Һ��BaCl2��Һ��Na2CO3��Һ
D.Ba��NO3��2��NaOH��Һ��Na2CO3��Һ
E.BaCl2��Һ��Na2CO3��Һ��NaOH��Һ
��2������̼������Һ�������� ��
��3��ϴ�Ӿ������ʹ�õIJ��������� ��
��4�������ᾧ�IJ��������� ��
���𰸡�
��1��CE
��2�����������Ӻ����ı�����
��3���ձ���©����������
��4�����������в����ò���������Һ���ֹ���Ȳ�����Һ��ɽ��������д����������������߽�������Һ��ʱ��ֹͣ���ȣ��������Ƚ�Һ������
���������⣺��1����ȥ��ҺI�е�MgCl2��CaCl2��Na2SO4 �� Ӧ���ǵ������Բ������µ����ʣ����Դ��ṩ���Լ���ѡNa2CO3��Һ��NaOH��Һ��BaCl2��Һ���ӹ������Ȼ�����ȥ��������ӣ�Ȼ����̼����ȥ�������Ӻ����ı����ӣ����������ƺ��Ȼ������Ⱥ�˳��Ҫ�����Կ����е�˳��BaCl2��Һ��Na2CO3��Һ��NaOH��Һ��NaOH��Һ��BaCl2��Һ��Na2CO3��Һ��BaCl2��Һ��Na2CO3��Һ��NaOH��Һ����CE��ȷ�����Դ��ǣ�CE����2���ӹ������Ȼ�����ȥ��������ӣ�Ȼ����̼����ȥ�������Ӻ����ı����ӣ����Դ��ǣ����������Ӻ����ı����ӣ���3��ϴ�Ӿ�������õ����ǹ�������װ�ã��õ��IJ��������У��ձ���©���������������Դ��ǣ��ձ���©������������4�������ᾧ���������н��У��������������̨����Ȧ�ϣ�����Һ�岻�����������ݻ���2/3������ʱ�����ò���������Һ���ֹ���Ȳ�����Һ��ɽ��������д����������������߽�������Һ��ʱ��ֹͣ���ȣ��������Ƚ�Һ�����ɣ����Դ��ǣ�����ʱ�����ò���������Һ���ֹ���Ȳ�����Һ��ɽ��������д����������������߽�������Һ��ʱ��ֹͣ���ȣ��������Ƚ�Һ�����ɣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к��е������ᣨ��ṹ��ʽ���£�������ƻ�����нϺõı���Ч����������һ��ʱ���ڷ�ֹ����ƻ�������ɫ������˵������ȷ���ǣ� �� 
A.������ķ���ʽ��C6H8O7
B.��������������ˮ���л���
C.����������к����Ȼ����ǻ�
D.������ֻ�ܷ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����Ҫ�Ļ���ԭ�ϣ�Ҳ��Ӧ�ù㷢�Ļ�����Ʒ��CO2��������ƻ������ط�Ӧ�ɲ���������
������м��㣺
��1��CO2ͨ�백ˮ����NH4HCO3 �� NH4HCO3�����ֽ⣮2.00mol NH4HCO3��ȫ�ֽ⣬�ֽ���ᆳ���������ΪL����״������
��2��ijH2�к���2.40molCO2 �� �û������ͨ��2.00L NaOH��Һ�У�CO2����ȫ���գ����NaOH��ȫ��Ӧ����NaOH��Һ��Ũ��Ϊ ��
��3��CO2��KO2�����з�Ӧ��
4KO2+2CO2��2K2CO3+3O2
4KO2+4CO2+2H2O��4KHCO3+3O2
��9mol CO2���ܷ���ں�KO2��Ӧ������9mol O2 �� ��Ӧǰ�ܷ����H2O����Ӧ���Ƕ��٣���ʽ���㣮
��4�������ˮ������Ӧ�IJ����Ǻϳɼ״���ԭ�ϣ�CH4+H2O ![]() CO+3H2 �� ��֪��CO+2H2
CO+3H2 �� ��֪��CO+2H2![]() CH3OH CO2+3H2
CH3OH CO2+3H2![]() CH3OH+H2O��300mol CH4��ȫ��Ӧ��IJ����У�����100mol CO2��ϳɼ״�������ü״�350mol����������120mol������CO2��ת���ʣ�
CH3OH+H2O��300mol CH4��ȫ��Ӧ��IJ����У�����100mol CO2��ϳɼ״�������ü״�350mol����������120mol������CO2��ת���ʣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������AgCl(s)�ֱ����ӵ�����������Һ�У�������Һc��Ag+����С����
A.10 mL 0.4mol��L-1������B.10 mL 0.3mol��L-1MgCl2��Һ
C.10 mL 0.5mol��L-1NaCl��ҺD.10 mL 0.1mol��L-1AlCl3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2CrO42��+2H+Cr2O72��+H2O��25��ʱ�����ڳ�ʼŨ��Ϊ1.0molL��1 ��Na2CrO4��Һ��pH���ⶨƽ��ʱ��Һ��c��Cr2O72������c��H+���������ͼ��ʾ�����ߣ�����˵������ȷ���ǣ� �� 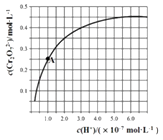
A.ƽ��ʱ��pHԽС��c��Cr2O72����Խ��
B.A��CrO42����ƽ��ת����Ϊ50%
C.A��CrO42��ת��ΪCr2O72����Ӧ��ƽ�ⳣ��K=1014
D.ƽ��ʱ������Һ��c��Cr2O72����=c��Cr2O42��������c��H+����2.0��10��7 molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z��ԭ������������������ֶ�����Ԫ�أ�W����̬�⻯����ʹ��ɫʯ����Һ������W��X����Ԫ�ص�����������ˮ���������Y�������������Ӧ��W��X��Y��Z������������֮��Ϊ16��
��1��W���ʵĵ���ʽ�� ��
��2�����û�ѧ�������W����̬�⻯����ʹ��ɫʯ����Һ������ԭ�� ��
��3����֪AsԪ�ص�ԭ������Ϊ33����W��ͬһ���壬As��Ԫ�����ڱ��е�λ���� ��
��4��W������������ˮ������Y�������������Ӧ�����ӷ���ʽ��
��5��X��Z�ĵ���֮�䷢����Ӧ�Ļ�ѧ����ʽ�� ��
��6����֪Q��Z��λ���������ڵ�ͬ����Ԫ�أ�ij�¶��£�����Ԫ�ص���̬������H2�������Ϸ�Ӧ������̬�⻯���ƽ�ⳣ���ֱ�ΪKQ=5.6��107 �� KZ=9.7��1012 �� Q��Ԫ�ط����� �� ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�й����ʣ����ɶ�����Ԫ���γɣ�֮���ת����ϵ������AΪ�����Ľ������ʣ�BΪ�ǽ������ʣ�һ���Ǻ�ɫ��ĩ����C�dz�������ɫ��ζҺ�壬D�ǵ���ɫ�Ĺ��廯�������Ӧ����ͼ����ʡ�ԣ� 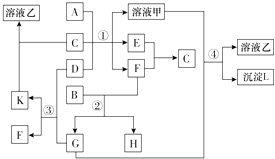
��1��A��B��C��D���������ʷֱ�Ϊ���������ѧʽ����
��2����Ӧ���е�C��D���������÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3����Ӧ�ܵ����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᵽ�������У����ε�ˮ���ص���
A.������FeCl3������ˮ��
B.Ϊ����FeCl3��Һ��Ҫ����Һ�м���������
C.��NaHCO3��Al2(SO4)3������Һ������ĭ����
D.������������Լ�ƿ��������ò����Լ�ƿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǻ�����ij��Ӧ�Ļ�ѧ��Ӧ�����淴Ӧʱ��仯��ʾ��ͼ������������ʾ��ͼ������ϵ��ǣ� �� 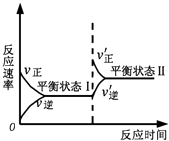
A.��Ӧ��ƽ��ʱ������Ӧ���ʺ��淴Ӧ�������
B.�÷�Ӧ�ﵽƽ��״̬���С��Ӧ��Ũ�ȣ�ƽ�ⷢ���ƶ����ﵽƽ��״̬��
C.�÷�Ӧ�ﵽƽ��״̬�������Ӧ��Ũ�ȣ�ƽ�ⷢ���ƶ����ﵽƽ��״̬��
D.ͬһ�ַ�Ӧ����ƽ��״̬���ƽ��״̬��ʱŨ�Ȳ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com