
【题目】高铁酸钠(Na2FeO4)具有优良的杀菌效果,是一种理想的含氯杀菌剂替代品。以低碳钢板作为阳极电解浓氢氧化钠可以迅速制得高铁酸钠,其工作原理如图所示。下列说法正确的是
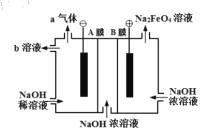
A.“A膜”、“B膜”分别为阴、阳离子交换膜
B.阴极区溶液的pH将减小
C.a气体为H2,,b溶液可循环使用
D.阳极反应为:![]()
【答案】C
【解析】
以低碳钢板作为阳极电解浓氢氧化钠制得高铁酸钠,阳极反应为![]() ,阳极消耗OH-,所以B膜为阴离子交换膜,允许OH-通过,阴极反应为:
,阳极消耗OH-,所以B膜为阴离子交换膜,允许OH-通过,阴极反应为:![]() ,阴极产生OH-,所以A膜为阳离子交换膜,允许钠离子通过。
,阴极产生OH-,所以A膜为阳离子交换膜,允许钠离子通过。
A. 根据题意,阳极反应为![]() ,阳极消耗OH-,所以B膜为阴离子交换膜,允许OH-通过,阴极反应为:
,阳极消耗OH-,所以B膜为阴离子交换膜,允许OH-通过,阴极反应为:![]() ,阴极产生OH-,所以A膜为阳离子交换膜,允许钠离子通过。即 “A膜”、“B膜”分别为阳、阴离子交换膜,A项错误;
,阴极产生OH-,所以A膜为阳离子交换膜,允许钠离子通过。即 “A膜”、“B膜”分别为阳、阴离子交换膜,A项错误;
B. 阴极反应为:![]() ,产生OH-,故溶液的pH将变大,B项错误;
,产生OH-,故溶液的pH将变大,B项错误;
C. 阴极反应为:![]() ,所以a气体为H2,,b溶液为浓的氢氧化钠可循环使用,C项正确;
,所以a气体为H2,,b溶液为浓的氢氧化钠可循环使用,C项正确;
D. 阳极反应为:![]() ,D项错误。
,D项错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:______________________________________________。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是________反应。
(2)甲和乙两个水浴作用不相同。
甲的作用是__________________________;乙的作用是__________________________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________________。集气瓶中收集到的气体的主要成分是__________________________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有__________。要除去该物质,可先在混合液中加入________________(填写字母)。
a.氯化钠溶液 b.苯
c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________________(填实验操作名称)即可除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。回答下列问题:
(1)Fe的价层电子排布式为___。
(2)Li、F、P、As四种元素的电负性由大到小的顺序为___。
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是___。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
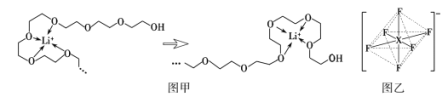
①聚乙二醇分子中,碳、氧的杂化类型分别是___、___。
②从化学键角度看,Li+迁移过程发生___(填“物理变化”或“化学变化”)。
③PF6中P的配位数为___。
④相同条件,Li+在___(填“LiPF6”或“LiAsF6”)中迁移较快,原因是___。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的品胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为___。LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则LiCl·3H2O晶体的密度为___g·cm-3(列出计算表达式)。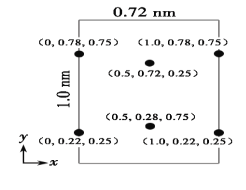
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一密闭容器中存在反应:![]() △H,实验测得平衡时Fe3O4的转化率α随温度和压强的变化如图所示。下列说法正确的是
△H,实验测得平衡时Fe3O4的转化率α随温度和压强的变化如图所示。下列说法正确的是
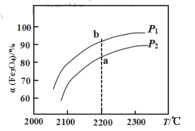
A.该反应的△H<0
B.压强PI<P2
C.将O2不断分离出去可以提高Fe3O4的转化率
D.a、b两点的平衡常数大小:Ka<Kb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:
(1)2A(g) ![]() 2B(g)+C(g); (2)A(g)
2B(g)+C(g); (2)A(g) ![]() C(g)+D(g)。
C(g)+D(g)。
当达到平衡时,测得c(A)=2.5 mol·L-1(表示该物质浓度,下同),c(C)=2.0 mol·L-1。则下列说法中正确的是( )
A.达到平衡时A的总转化率为40%B.达到平衡时c(B)为1.0 mol·L-1
C.达到平衡时c(B)=2c(D)D.达到平衡时c(D)=2c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是一种重要的化工原料。工业中以乙苯![]() 为原料,采用催化脱氢的方法制取苯乙烯
为原料,采用催化脱氢的方法制取苯乙烯![]() 。回答下列问题:
。回答下列问题:
己知:①![]()
![]()
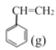 +H2(g) △H1>0
+H2(g) △H1>0
②![]() △H2>0
△H2>0
(1)![]() +CO2(g)
+CO2(g)![]()
![]() +CO(g)+H2O(g) △H=_______,(用△H 1、△H 2表示)有利于提高己苯平衡转化率的条件是____(填标号)。
+CO(g)+H2O(g) △H=_______,(用△H 1、△H 2表示)有利于提高己苯平衡转化率的条件是____(填标号)。
a 高温 b 高压 c 低温 d 低压
(2)已知T1℃下,将1mol乙苯蒸气通入到体积为2L的密闭容器中进行反应①,容器内气体总物质的量随反应时间的变化情况如下表所示:
时间t/min | 0 | 10 | 20 | 30 | 40 |
总物质的量n/mol | 1.0 | 1.4 | 1.65 | 1.8 | 1.8 |
①由表中数据计算0~10min内v(H2)=____:平衡时乙苯的转化率为____
②T1℃下该反应的平衡常数K1=____
③若温度T1℃下的平衡常数K小于T2℃下的平衡常数K2,则T1____T2(填“>”、 “<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NaIO3+5SO2+4H2O=I2+3H2SO4+2NaHSO4,利用下列装置从含NaIO3的废液中得到I2的苯溶液并回收NaHSO4。其中装置正确且能达到相应实验目的的是( )
A.制取SO2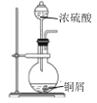
B.还原IO3-
C.放出I2的苯溶液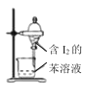
D.从水溶液中提取NaHSO4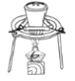
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不发生消去反应的是( )
①![]() ②
② ③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤
③(CH3)3CCH2Cl ④CHCl2-CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A.①③⑥B.②③⑤C.全部D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1000 mol/L NaOH溶液滴定20.00 mL 0.1000 mol/L HCl溶液过程中的pH变化如图所示。下列说法错误的是
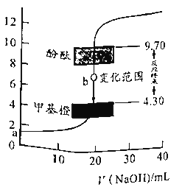
A.b点时,加入极少量NaOH溶液都会引起pH的突变
B.选指示剂时,其变色范围应在4.30~9.70之间
C.若将HCl换成同浓度的CH3COOH,曲线ab段将会上移
D.都使用酚酞做指示剂,若将NaOH换成同浓度的氨水,所消耗氨水的体积较NaOH小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com