
【题目】下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。
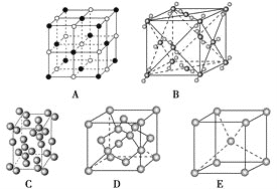
(1)辨别晶胞(请用相应的编号填写)。
①钠晶胞是________;
②碘晶胞是________;
③金刚石晶胞是________;
④干冰晶胞是________;
⑤氯化钠晶胞是________。
(2)与冰的晶体类型相同的是__________。
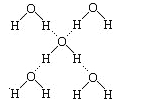
(3)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ·mol-1,除氢键外,水分子间还存在范德华力(11 kJ·mol-1),则冰晶体中氢键的“键能”是________kJ·mol-1。
【答案】E C D B A BC 20
【解析】
由晶胞图可知,A为氯化钠的晶胞图,构成微粒为离子;B为干冰的晶胞图,构成微粒为二氧化碳分子;C为碘的晶胞图,构成微粒为碘分子;D为金刚石的晶胞图,构成微粒为碳原子;E为钠的晶胞图,构成微粒为原子。
(1)由分析可知,A为氯化钠的晶胞图,B为干冰的晶胞图,C为碘的晶胞图,D为金刚石的晶胞图,E为钠的晶胞图;
(2) 金刚石属于原子晶体、氯化钠属于离子晶体,钠是金属晶体,碘和干冰属于分子晶体。冰属于分子晶体,故与冰的晶体类型相同的是BC;
(3) 每个水分子与相邻的4个水分子形成氢键,每个氢键属于水分子的1/2,所以1mol冰晶体中含有2mol氢键,冰吸收热量升华,成为水蒸气,需要克服2mol氢键和范德华力,设氢键的“键能”是x,所以51kJ/mol=11kJ/mol+2x,解得x=20kJ/mol。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】现有三种可溶性物质A、B、C,其中A、B属于盐,C属于碱,它们溶于水后电离产生的所有离子如下表所示:
阳离子 | Na+ H+ Ba2+ |
阴离子 | OH- CO32- SO42- |
请根据下列叙述回答问题:
(1)C的化学式为___。
(2)A溶液与B溶液反应可生成气体X,则X的化学式为___,该反应的离子方程式为___。
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为___,鉴别溶液中B的阴离子的试剂为___。
②D溶于稀硝酸的离子方程式为___。
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下体积为VL,则E在混合物中的质量分数的表达式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氢硫酸是一种二元弱酸,请回答以下问题:
(1)已知 0.1mol/L NaHS 溶液显碱性,则c(S2—)___c(H2S)(填“>”“<”或“=”)。
(2)常温下,向 0.2mol/L的 H2S溶液中逐滴滴入 0.2mol/L NaOH 溶液至中性,此时溶液中以下所示关系不正确的是___(填字母)。
A. c(H+)·c(OH-)=1×10-14
B. c(Na+)=c(HS—)+2c(S2—)
C. c(Na+)> c(HS—)+c(S2—)+ c(H2S)
D. c(H2S)> c(S2—)
(3)已知常温下,CaS 饱和溶液中存在平衡CaS(s) ![]() Ca2+(aq)+S2-(aq) △H>0。
Ca2+(aq)+S2-(aq) △H>0。
①温度升高时,KSP(CaS ) =___ (填“增大”“减少”或“不变”,下同)。
②滴加少量浓盐酸时,c(Ca2+ )___,原因是___(用文字和离子方程式说明)。
③若向CaS 饱和溶液中加入Cu(NO3)2 溶液中,生成一种黑色固体物质,写出该过程中反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述变化理论上计量结果正确的是( )
A. 标准状况下,用含空气和氨气体积各半的烧瓶进行喷泉实验,所得溶液的物质的量浓度约为![]()
B. 相同质量的两份铝,分别放入足量的![]() 和
和![]() 溶液中充分反应,消耗的
溶液中充分反应,消耗的![]() 和
和![]() 之比为1∶1
之比为1∶1
C. 将![]() 逐滴加入到
逐滴加入到![]() 溶液中,产生
溶液中,产生![]() 的体积约为
的体积约为![]() (标准状况下)
(标准状况下)
D. 向![]() 的
的![]() 溶液中通入足量的
溶液中通入足量的![]() 气体,生成
气体,生成![]() 沉淀
沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验:加热钠至熔化后,停止加热并通入氯气,钠剧烈燃烧并生成大量白烟。以下叙述错误的是
![]()
A.棉花球处发生的离子反应是Cl2+H2O = H++Cl-+HClO
B.大量白烟是氯化钠固体小颗粒
C.钠着火燃烧产生黄色火焰
D.可在棉花球右侧用湿润的淀粉KI试纸判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是盛放浓硫酸试剂瓶标签上的部分内容。现用该浓硫酸配制240 mL 1.0 mol·L-1的稀硫酸。请回答下列问题:

(1)配制上述稀硫酸时,可供选用的仪器有:①玻璃棒;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦胶头滴管。还缺少的仪器有______________(写仪器名称);
(2)容量瓶上除有刻度线外还应标有____________,在使用前必须检查容量瓶是否____________。
(3)配制240 mL 1.0 mol·L-1的稀硫酸需要用量筒量取上述浓硫酸,量取浓硫酸时应选用以下_____规格的量筒(填选项)。
A.10 mL B.25 mL C.50 mL D.100 mL
(4)配制过程有以下操作:
A.移液 B.量取 C.洗涤 D.定容 E.稀释 F.摇匀 G.计算
其正确的操作顺序应是______________(填序号)。
(5)经过测定,某同学配制的稀硫酸浓度偏低,则可能的原因是_______(填序号)
①用量筒量取浓硫酸时,仰视刻度线
②容量瓶用蒸馏水洗涤后未经干燥
③洗涤烧杯内壁和玻璃棒后将洗涤液倒入废液缸
④转移溶液时,不慎有少量溶液洒出
⑤定容时,俯视容量瓶刻度线
⑥摇匀后发现溶液的凹液面低于刻度线,再加蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol MnO2和100 mL 12 mol·L-1盐酸混合后缓缓加热,生成气体单质A,反应完全后向留下的溶液中加入足量AgNO3溶液 (不考虑盐酸的挥发) 。下列说法错误的是
A.在生成气体A的反应中,MnO2是氧化剂,盐酸是还原剂
B.气体单质A是氯气,它的体积是2.24L
C.生成AgCl沉淀的物质的量为1mol
D.整个反应过程被氧化的盐酸有0.4mol,并转移了0.2mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加徳罗常数的值,诺贝尔物理学奖获得者让·佩兰于 1909 年提出常数命名 为阿伏加德罗常量来纪念他,下列说法正确的是
①标准状况下,11.2 L 以任意比例混合的氮气和氧气所含的原子数为 NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③2 mol/L 的氯化镁溶液中含氯离子数目为 4 NA
④标准状况下,22.4 L 水中分子数为 NA
⑤46 g NO2 和 N2O4 混合气体中含有原子数为 3 NA
A.①②⑤B.①②C.①③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应4HCl(g)+O2(g)═2Cl2(g)+2H2O(g),已知2 mol O2被还原时,放出a kJ的热量,且知断开1 mol O=O键需要吸收b kJ的热量,断开1 mol Cl—Cl键需要吸收c kJ的热量。则断开1 mol H—O键比断开1 mol H—Cl键所需能量高
A. (b-a-2c)/4kJB. (a+2b-4c)/8kJC. (a+b-2c)/4kJD. (2b-a-4c)/8kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com