
【题目】298 K时,分别向体积、浓度均为20mL0.1mol·L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示。(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )

A. 298K 时,0.1mol·L-1HX 溶液中HX的电离度为1%
B. V=10mL时,同时微热溶液(忽略体积变化),  逐渐增大
逐渐增大
C. V=20mL 时,HX曲线对应的溶液中c(Na+)=c(X-)>c(H+)=c(OH-)
D. 滴定这两种溶液时都可以选择甲基橙替代酚酞作指示剂
科目:高中化学 来源: 题型:
【题目】现有48.4 g碱式碳酸镁样品(化学式:xMgCO3·yMg(OH)2·zH2O,x、y、z为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入150 mL某浓度的盐酸中,充分反应后生成CO2 4.48 L(已折算成标准状况下),所得溶液稀释至250 mL,测得溶液的c(H+)=0.100 mol·L-1。
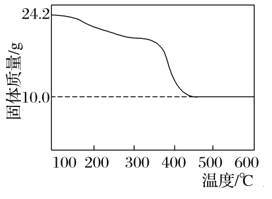
按要求回答下列问题:
(1)盐酸的物质的量浓度c(HCl)=________mol·L-1。
(2)x∶y∶z=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法正确的是( )
A. 燃煤中加入生石灰可以减少酸雨的形成及温室气体的排放
B. 对医疗器械高温消毒时,病毒蛋白质受热变性
C. 钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高
D. NaHCO3能与碱反应,因此食品工业上可用作焙制糕点的膨松剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO2(含有杂质MnO和MnCO3)制取纯MnO2的流程如下:

请回答下列问题:
(1)为加快酸浸速率可采取的措施有______________________________________(答两点)。酸浸过程中稀硫酸可否用盐酸代替,回答并说明理由_________________________。
(2)操作X的名称是____________。氧化过程反应的离子方程式是________________。
(3)加热条件下Cl2与NaOH溶液反应,其氧化产物和还原产物的物质的量之比为________。
(4)酸浸过程中得到的溶液所含主要溶质为____________,电解该溶液也可制得MnO2和H2,写出该电解过程中阳极的电极反应式________________________________。
(5)MnO2常用作某些化学反应的催化剂。下图为2H2O2=2H2O+O2↑反应过程中的能量变化示意图,下列说法正确的是__________。

a.该反应为吸热反应,热效应为△H
b.反应历程b有催化剂参加
c.有催化剂时,该反应的活化能为E1+E2
d.改变催化剂,可改变该反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系正确的是( )
A. 密度:CCl4>CHCl3>H2O
B. 熔点:2,3一二甲基丁烷>2一甲基丁烷>戊烷
C. 同质量的物质完全燃烧耗O2量:乙烯>乙炔>甲烷
D. 同物质的量物质完全燃烧耗O2量:环已烷>苯>苯甲酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在日常生活中有着广泛的应用。下列说法不正确的是
A. 炒菜时加碘食盐最好最后放
B. 明矾可用于水的杀菌消毒
C. 雾霾天气中可以产生丁达尔现象
D. 燃料的脱硫和脱氮都是减少酸雨产生的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见的有机物的转化关系。下列说法错误的是( )

A. 反应①、③均属于加成反应 B. 乙酸与甲酸甲酯互为同分异构体
C. 乙醇溶液可除去暖瓶中的水垢 D. 反应④、⑤、⑥、⑦均属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:

已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
![]()
回答以下问题:
(1)A中含有的官能团名称是_________________________________。
(2)写出F生成G的化学方程式____________________________________。
(3)写出J的结构简式__________________________________。
(4)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式______。
①FeCl3溶液发生显色反应 ②能发生银镜反应
③苯环上只有两个对位取代基 ④能发生水解反应。
(5)参照上述合成路线,设计一条由乙醛(无机试剂任选)为原料合成二乙酸-1,3-丁二醇酯(![]() )的合成路线_____________。
)的合成路线_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知钡的金属活动性介于钠和钾之间,下列叙述中正确的是( )
A. 钡与水反应不如钠与水反应剧烈 B. 钡可以从NaCl溶液中置换出钠
C. 氧化性:K+>Ba2+>Na+ D. 碱性:KOH>Ba(OH)2>NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com