
【题目】(1)对于反应:2SO2(g)+O2(g)![]() 2SO3 (g) ,下面表示该反应速率最快的是_______。
2SO3 (g) ,下面表示该反应速率最快的是_______。
A.v(SO2)= 2 mol/(L·min) B.v(O2)=1mol/(L·min)
C.v(O2)=2mol/(L·min) D.v(SO3)= 3mol/(L·min)
(2)下图表示在密闭容器中反应:2SO2(g)+O2(g)![]() 2SO3 (g) ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a b过程中改变的条件是______________;
2SO3 (g) ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a b过程中改变的条件是______________;
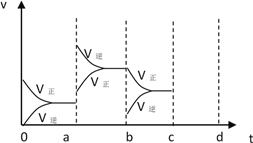
b c过程表示平衡向_______方向移动; 若增大压强时,反应速率变化情况画在下图c~d处______________.
【答案】 C 升高温度 正 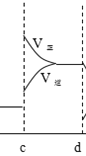
【解析】(1)利用归一法计算,即速率比等于计量数之比,将速率都归一为v(SO2),C.v(O2)=2mol/(L·min),v(SO2)= 4 mol/(L·min) ;D.v(SO3)= 3mol/(L·min),v(SO2)= 3 mol/(L·min),C最快。
(2)a时逆反应速率大于正反应速率,且正逆反应速率都增大,说明平衡应向逆反应方向移动,该反应的正反应放热,应为升高温度的结果;b时正反应速率不变,逆反应速率减小,在此基础上逐渐减小,应为减小生成物的原因,平衡向正反应方向移动;若增大压强时,平衡向正反应方向移动,则正逆反应速率都增大,且正反应速率大于逆反应速率,图象应为:
 。
。


科目:高中化学 来源: 题型:
【题目】据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解质溶液为KOH溶液。下列有关该电池的叙述不正确的是
A. 正极反应式为:O2+2H2O+4e-=4OH-
B. 工作一段时间后,电解质溶液中KOH的物质的量不变
C. 该燃料电池的总反应方程式为:2H2+O2=2H2O
D. 用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以烯烃为原料,合成某些高聚物的路线如下:
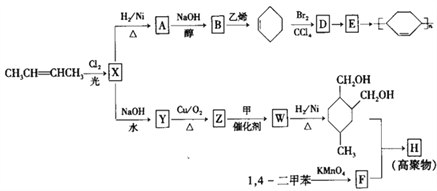
已知: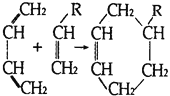 (或写成
(或写成![]() )
)
(1)CH3CH=CHCH3的名称是____________。
(2)X中含有的官能团是______________。
(3)A→B的化学方程式是_____________。
(4)D→E的反应类型是_______________。
(5)甲为烃,F能与NaHCO3反应产生CO2。
①下列有关说法正确的是_______________。
a.有机物Z能发生银镜反应 b.有机物Y与HOCH2CH2OH互为同系物
c.有机物Y的沸点比B低 d.有机物F能与己二胺缩聚成聚合物
②Y的同分异构体有多种,写出分子结构中含有酯基的所有同分异构体的种类数_____。
③Z→W的化学方程式是__________________。
(6)高聚物H的结构简式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaSO4在医疗上可做消化系统造影剂,2mol BaSO4含有的硫原子个数为
A. 2 B. 2×6.02×1023 C. 6 D. 6×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL 0.3mol/L Na2SO4溶液和50mL 0.2mol/L Al2(SO4)3溶液混合后,溶液中SO42﹣的物质的量浓度约为( )
A.0.20mol/L
B.0.25mol/L
C.0.4mol/L
D.0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通式为CnH2n-2的一种气态炔烃完全燃烧后,生成CO2和H2O的物质的量之比为4:3,则这种烃的链状同分异构体有( )
A.5种B.4种C.3种D.2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是
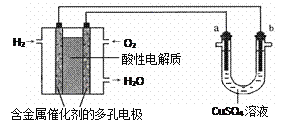
A. 燃料电池工作时,通入氢气的是正极
B. a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D. a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com