
 ϡ��Һ�У�
ϡ��Һ�У� ��
�� ����֪
����֪ ����
���� ��ϡ������
��ϡ������ ��
�� ��Һ��Ϻ���Һ��pH=_________����ʱ����Һ����ˮ�����
��Һ��Ϻ���Һ��pH=_________����ʱ����Һ����ˮ����� =_________��
=_________�� ���
��� ��ijǿ����Һ��1���
��ijǿ����Һ��1��� ��ijǿ����Һ��Ϻ���Һ�����ԣ�����ǰ����ǿ���
��ijǿ����Һ��Ϻ���Һ�����ԣ�����ǰ����ǿ��� ��ǿ���
��ǿ���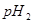 ֮��Ӧ����Ĺ�ϵ��_________��
֮��Ӧ����Ĺ�ϵ��_________��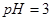 ��������Һ��
��������Һ�� ��
�� ��Һ�������Ϻ����Һ��
��Һ�������Ϻ����Һ�� _________����>7��=7��<7����
_________����>7��=7��<7����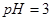 �Ĵ�����Һ��
�Ĵ�����Һ�� ��
�� ��Һ�������Ϻ����Һ��
��Һ�������Ϻ����Һ�� _________����>7��=7��<7����
_________����>7��=7��<7����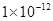
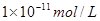
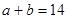 ����
����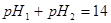 ��
��

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
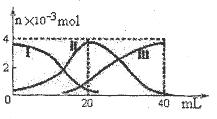
| A����V(NaOH)=20mLʱ����Һ������Ũ�ȴ�С��ϵ�� C(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| B��HA-�ĵ���̶�С��ˮ��̶� |
| C���μӹ����е���Һ������ʱ��V(NaOH)<20mL |
| D����V(NaOH)=40mLʱ����������Һ��ˮϡ�͵Ĺ�����pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���к�ʱ����NaOH����ǰ�߶� |
| B������ý�����Ӧʱ����ʼ������� |
| C��0.1mol/L�Ĵ�����Һ��H+��Ũ���� 0.01mol/L�Ĵ�����Һ��H+Ũ�ȵ�10��ѧ |
| D������̶Ⱥ��ߴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��aһ������0.01 |
| B����Ӧ����Һ��һ����c��Na+��+c(H+)=c(OH-)+c(CH3COO-) |
| C����Ӧ����Һ��һ����c(CH3COO-)+c(CH3COOH)>c(Na+) |
| D����Ӧ����Һ��һ����c(Na+)>c(CH3COO-)>c(H+)=c(OH) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��H2S 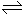 2H�� + S2- 2H�� + S2- | B��HF = H�� + F- |
| C��NaHSO3 = Na�� + H�� +SO32- | D��H2CO3+ H2O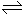 H3O+ + HCO3- H3O+ + HCO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3COO����H���У�Ҫʹ����ƽ��������c(H��)����Ӧ��ȡ�Ĵ�ʩ��(����)
CH3COO����H���У�Ҫʹ����ƽ��������c(H��)����Ӧ��ȡ�Ĵ�ʩ��(����)| A������NaOH(s) | B���������� | C��������ˮ | D�������¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaNO2��Һ��pH����7 |
| B����HNO2��Һ�м���NaNO2���壬��Һ��PH��� |
| C��������0.1mol/LHNO2��Һ��pHΪ2.1 |
| D����HNO2��Һ���������飬���ݺܰ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
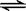 H����CH3COO���������������й���������ʹƽ�������ƶ�����
H����CH3COO���������������й���������ʹƽ�������ƶ�����| A��NaCl | B��Na2CO3 | C��CH3COONa | D��NaOH |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com