
��7�֣�����HNO3����ʱ����ԭ�������HNO3Ũ���й��⣬�����¶��йء���֪�������ϡHNO3��Ӧʱ����Ҫ��ԭ����ΪNO���壻���ȵ�ϡHNO3��Ӧʱ����Ҫ��ԭ����ΪN2O���壻��HNO3��ϡʱ������Ҫ��ԭ������NH4+����������ϡ HNO3�����ã��������ͼ���ش��й����⡣�������ߵĸ�����ֻ��һ�ֻ�ԭ���
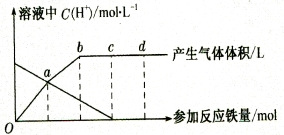
��1��0�㵽a��Ļ�ԭ������ ��
��2��a�㵽b��Ļ�ԭ������ ����ԭ������� ��
��3�������b�㵽c��ķ�Ӧ����ʽ��
��Fe+��HNO3������Fe( NO3)3+��[ ]+��H2O
��4����Ӧ�����У����� ��ʱ��HNO3����ȫ��Ӧ��
��5����֪�ﵽd��ʱ��Ӧ��������ʱ��Һ�е���Ҫ��������Fe2+����c���d��μӷ�Ӧ���������ʵ���֮���� ��
��7�֣�
��1�� NO ��1�֣� ��2�� N2O ��1�֣�����Ӧ���ȣ�ʹ��Һ�¶����� �������������𰸣���1�֣�
��3�� 8 30 8 3 NH4 NO3 9 ��2�֣� ��4�� c ��1�֣� ��5��2:3��1�֣�
��������
�������������Ŀ��Ϣ��֪����Ӧ��ʼʱ���¶Ƚϵͣ�������NO�����ŷ�Ӧ�Ľ��У����ڷ�Ӧ���ȣ��¶����ߣ����ɵIJ���ΪN2O����Ӧ�������У�����Ũ�Ƚ��ͣ�����ΪNH4 NO3 ������c��ʱ��c��H+��Ϊ0�����ᷴӦ��ȫ����ʱ��Һ������ΪNH4 NO3��Fe( NO3)3 ����Ӧ����d��ʱ����Ӧ��������Һ������ΪNH4 NO3��Fe( NO3)2 ���μӷ�Ӧ���������ʵ���֮�Ȳ�2��3.
���㣺��������ķ�Ӧ



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ����������и߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У�һ������ͬϵ�����
A���Ҷ����ͱ����� B�� C6H5��OH��C6H5��CH2OH
C��C3H6��C4H8 D��C2H6��C3H8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ����������и߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ʵ�顱���м��ס����㡢��Լ����ɫ���ŵ㣬�۲������ĸ������ʵ�顱���г�װ��δ
���������ж�����˵����ȷ���ǣ� ��
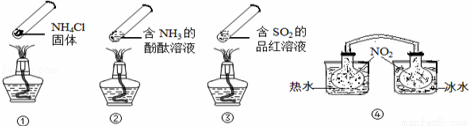
A������ʱ�����ϲ��㼯�˹���NH4Cl��˵��NH4Cl�����ȶ��ԱȽϺ�
B������ʱ���ڡ�����Һ����죬��ȴ���ֶ���Ϊ��ɫ
C������,��������ˮ�е�������������ɫ����,�����ڱ�ˮ�е�������������ɫ��dz
D���ĸ������ʵ�顱���������Ļ�ѧ��Ӧ���ǿ��淴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����п����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪ͬ�¶��£�������ĵ���ƽ�ⳣ���Ĵ�С��ϵΪKa��HX��>Ka��HY��>Ka��HZ���������ʵ���Ũ����ͬ��������NaX��NaY��NaZ��ҺpH�ɴ�С��˳����
A��NaX NaY NaZ B��NaX NaZ NaY
C��NaY NaZ NaX D��NaZ NaY NaX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����п����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��������ˮ�����ʵ��ܽ��Ϊ0
B��H+��OH����ˮ��Һ�л��ʱ����Ӧ�Ļ�ܼ���Ϊ0
C�����Ѵ�ƽ��Ŀ��淴Ӧ��v������=v���棩=0
D�������£�1mol/L��CH3COOH��Һ��pH=0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ײʱ,��ȫ�����з�����Ӧ10NaN3+2KNO3=K2O+5Na2O+16N2��������������Ȼ�ԭ�����1.75 mol���������ж���ȷ����
������42.0 L N2(��״��)
����0.250 mol KNO3������
��ת�Ƶ��ӵ����ʵ���Ϊ1.25 mol
�ܱ�������Nԭ�ӵ����ʵ���Ϊ3.75 mol
A���٢� B���ۢ� C���ڢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ͬ���ܱ������зֱ����O2��O3���壬��������������������¶Ⱥ��ܶ����ʱ������˵������ȷ����
A�����������ѹǿ���
B�������������ԭ�������
C����������ķ�����Ŀ���
D��O2��O3����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���£����и���������ָ����Һ���ܴ����������
A��pH=1����Һ�У�I-��NO3-��SO42-��Na+
B����ˮ�����c(H+)=1��10-14mol/L����Һ�У�Ca2+��K+��Cl-��HCO3-
C��c(H+)/c(OH-)=1012����Һ�У�NH4+��Al3+��NO3-��Cl-
D��c(Fe3+)=0��1mol/L����Һ�У�K+��ClO-��SO42-��SCN-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������人�������и߶�10���¿���ѧ���������Ծ��������棩 ���ͣ�ѡ����
a mol N2��b mol H2��ϣ�Ҫһ�������·�Ӧ�ﵽƽ�⣬������c mol NH3����NH3��ƽ����ϵ����������Ϊ�� ��
A�� B��
B�� 
C�� D��
D��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com