
【题目】工业合成氨以及含氮废水的处理一直是工业研究的热点。回答下列问题:
(1)已知:氢气的燃烧热为-285.8kJ/mol,17g氨气在纯氧中燃烧生成氮气和液态水的过程中放热382.6kJ,则工业合成氨的热化学方程式为_________________。
(2)500℃时,在容积固定的密闭容器中模拟工业合成氢N2+3H2![]() 2NH3,下表为容器中部分物质浓度随时间的变化情况(其余浓度未给出)。
2NH3,下表为容器中部分物质浓度随时间的变化情况(其余浓度未给出)。
时间/min | c(N2)/mol/L | c(H2)/mol/L | c(NH3)/mol/L |
0 | 0.18 | 2.3 | 0 |
5 | 0.08 | ||
6 | 0.08 | ||
10 | 0.06 | 1.94 | 0.24 |
500℃时,该反应的化学平衡常数K=_______L2·mol-2;5min内,反应的平均速率v(H2)_____ mol·L-1·min-1;6min时,某一条件发生了改变,可能是_____(填序号)。
a.使用催化剂 b.降低温度 c.增加H2的浓度 d.分离出NH3
(3)无机含氮废水主要含有铵氮(NH4+)和硝氮(NO3-)。可使用电化学氧化法处理铵氮废水,原理是溶液中的NH4+直接在电极上放电生成无毒物质,该过程阳极上的电极反应式为_______________。为研究电化学氧化法去除铵氮的影响因素,在实验室中以石墨作电极模拟对高浓度铵氮废水进行电化学氧化处理,得到如下3组图像:



通过分析上述图像可知,最适宜选用的条件是___________、以及初始pH为11的碱性溶液。实验中,铵氮去除率总是高于总氮去除率的原因是__________________。
【答案】 N2(g)+3H2(g) ![]() 2NH3(g)△H=-92.2kJ/mol 6.25×10-2 0.06 b 2NH4+-6e-=N2↑+8H+ 电流密度为80mA·cm-2,极板间距为30mm 废水中除了铵氮外,可能还含有硝氮,不能通过氧化法去除
2NH3(g)△H=-92.2kJ/mol 6.25×10-2 0.06 b 2NH4+-6e-=N2↑+8H+ 电流密度为80mA·cm-2,极板间距为30mm 废水中除了铵氮外,可能还含有硝氮,不能通过氧化法去除
【解析】(1)氢气的燃烧热为-285.8kJ/mol,所以有反应①H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ/mol,17g氨气在纯氧中燃烧生成氮气和液态水的过程中放热382.6kJ,所以有反应②NH3(g)+3/4O2(g)=1/2N2(g) + 3/2H2O(l) △H=-382.6kJ/mol,所以①×3+②×(-2)得到:N2(g)+3H2(g) ![]() 2NH3(g)△H=-92.2kJ/mol。
2NH3(g)△H=-92.2kJ/mol。
(2)由表中数据得到,5~6分钟氮气的浓度不变,反应达平衡。根据表中数据可以计算出5分钟的时候N2、H2、NH3的浓度分别为:0.08mol/L、2mol/L、0.2mol/L,所以平衡常数K=![]() 。v(N2)=(0.18-0.08)/5=0.02 mol·L-1·min-1,所以v(H2)=3 v(N2)= 0.06 mol·L-1·min-1。10分钟时与6分钟的数据比较,氢气的浓度减小,所以不会是加入氢气,选项c错误;氨气的浓度增大,所以不会是分离出氨气,选项d错误;加入催化平衡应该不移动,选项a错误。降低温度平衡向正反应方向移动,所以氮气和氢气的浓度降低,氨气的浓度增大,选项b正确。
。v(N2)=(0.18-0.08)/5=0.02 mol·L-1·min-1,所以v(H2)=3 v(N2)= 0.06 mol·L-1·min-1。10分钟时与6分钟的数据比较,氢气的浓度减小,所以不会是加入氢气,选项c错误;氨气的浓度增大,所以不会是分离出氨气,选项d错误;加入催化平衡应该不移动,选项a错误。降低温度平衡向正反应方向移动,所以氮气和氢气的浓度降低,氨气的浓度增大,选项b正确。
(3)阳极应该发生失电子的氧化反应,铵根离子应该被氧化为氮气,所以阳极的反应为:2NH4+-6e-=N2↑+8H+。从三个图像得到,电流密度为80mA·cm-2,极板间距为30mm时,铵氮的去除率比较高。溶液中的总氮包括铵氮和硝氮,铵氮在这个过程中被氧化而除去,但是硝氮中的N是+5价,不可能氧化除去,所以铵氮去除率总是高于总氮去除率。


 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】已知 2Fe2+ +Br2 = 2Fe3+ + 2Br-;2 Br- + Cl2 = Br2 + 2Cl-;2Fe3+ + 2I-= 2Fe2+ + I2。向 FeI2、FeBr2 的 混合溶液中通入 Cl2,溶液中某些离子的物质的量 n(离子)随通入 Cl2 的物质的量 n(Cl2)变化如图所示。则下列有关说法中不正确的是( )
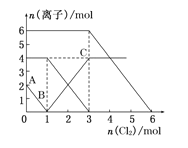
A. 还原性:I>Fe2+>Br
B. 原溶液中:n(Fe2+):n(I):n(Br)=2:1:3
C. 原混合溶液中 FeBr2 的物质的量为 6 mol
D. 当通入 2mol Cl2 时,溶液中已发生的离子反应可表示为:2Fe2++2I+2Cl2═2Fe3++I2+4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述中正确的是( )
A.化合反应一定是氧化还原反应
B.氧化还原反应的本质是元素化合价的升降
C.金属单质在化学反应中一定作还原剂
D.失电子的反应物在反应中作还原剂,反应中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子检验的方法正确的是( )
A.某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl-
B.某溶液中加Ba(OH)2溶液生成蓝色沉淀,说明原溶液中有Cu2+
C.某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中有SO42-
D.某溶液中加稀硫酸溶液产生无色气体,说明原溶液中有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,能大量共存的离子组是
A.K+、Na+、CO32-、NO3-B.Ag+、Na+、SO42-、Cl-
C.OH-、HCO3-、Ca2+、Na+D.Ba2+、Na+、OH-、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的钙离子、镁离子、硫酸根离子及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)第①步中,操作A是__________,第⑤步中,操作B是__________。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)____________________________。
(3)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因是_________________________。
(4)判断氯化钡已过量的方法是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ka(CH3COOH)=1.7×10-5,Kb(NH3·H2O)=1.7×10-5。25℃时,向40ml浓度均为0.01mol·L-1的盐酸和醋酸(1:1)混合溶液中逐滴加入0.10mol·L-1的氨水,测定过程中电导率和pH变化曲线如图所示,下列说法正确的是

A. a点溶液中,c(CH3COO-)数量级约为10-5
B. b点溶液中,c(NH4+) < c(CH3COOH)
C. c点溶液中,c(NH4+) > c(Cl-)+c(CH3COO-)
D. d点水的电离程度大于c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。A 是生活中一种常见的调味品,B 是最常见的无色液体,X、Y是两种常见的金属单质。D、E、F为气体,且 E为黄绿色,F能使品红溶液褪色,E 与 F 以等物质的量反应。请回答下列问题:
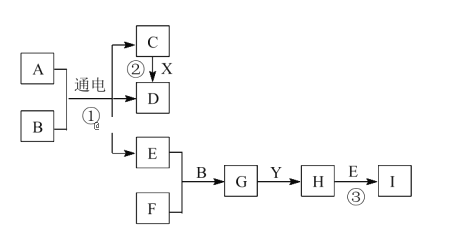
(1)F的化学式是________。溶液 G 中含有的主要离子为_____________(用离子符号表示)。
(2)反应②的化学方程式为___________________。
(3)反应③的离子方程式为________________________________。
(4)请补充完整检验H中阳离子的实验方案:取少量H中的溶液于试管中,_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com