
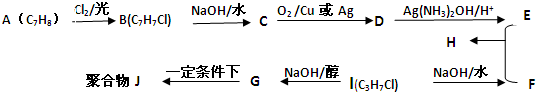
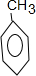
 ,B为
,B为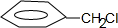 ,C为苯甲醇
,C为苯甲醇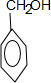 ,D为苯甲醛
,D为苯甲醛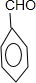 ,E为苯甲酸
,E为苯甲酸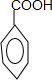 ;根据已知信息②结合I→F,I→G的反应条件可知,I为CH3CHClCH3,F为CH3CHOHCH3,G为CH2=CHCH3.
;根据已知信息②结合I→F,I→G的反应条件可知,I为CH3CHClCH3,F为CH3CHOHCH3,G为CH2=CHCH3. ,C为苯甲醇,D为苯甲醛,E为苯甲酸;
,C为苯甲醇,D为苯甲醛,E为苯甲酸; ,C为苯甲醇,故答案为:
,C为苯甲醇,故答案为: ;醇羟基;
;醇羟基;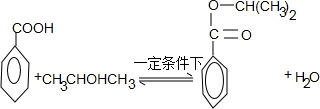 ,
, ;
;| 乙醇 |
| △ |
| 乙醇 |
| △ |
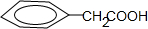 一种,
一种, 还有间位、对位3种,共4种;K的同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,说明有酚羟基和醛基,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,可见其在对位上,结构为:
还有间位、对位3种,共4种;K的同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,说明有酚羟基和醛基,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,可见其在对位上,结构为: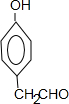 ,故答案为:4;
,故答案为:4; .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、室温时,1L pH=2的NH4Cl溶液中水电离出10-12mol H+ |
| B、常温常压下,46g NO2含有的原子数小于3NA |
| C、12g石墨含有4NA个自由移动的电子 |
| D、1mol LiAlH4在125℃完全分解成LiH、H2、Al,转移电子3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
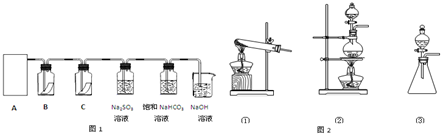
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
| 改变条件 | 速率变化 |
| 降低温度 | |
| 增加O2的浓度 | |
| 使用V2O5做催化剂 | |
| 压缩气体 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
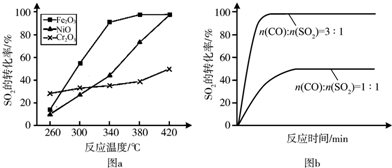
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
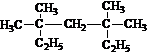 系统命名为
系统命名为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若向密闭体系内再加入3mol B、2mol C,达平衡时C的百分含量与原平衡相同 |
| B、达到平衡时气体的总物质的量、密度都不发生变化 |
| C、反应达平衡的过程中,释放出的热量不发生变化 |
| D、升高温度A的转化率大于30% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com