
【题目】下列说法正确的是( )
A﹒现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B﹒n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为35.5m/n
C﹒标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D﹒5.6 g CO和4.48 L CO2中含有的碳原子数一定相等
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述或操作中正确的是( )
A. 浓硫酸能使硫酸铜晶体失去结晶水,体现了浓硫酸的脱水性
B. 浓硫酸对有机物的腐蚀性是浓硫酸脱水性和强氧化性的综合体现
C. 浓硫酸具有氧化性,稀硫酸无氧化性
D. 浓硫酸不慎沾到皮肤上,应立即用布拭去,再涂上稀NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,也常用于鱼类、肉类等食品的染色和防腐,易溶于水,微溶于乙醇. 某化学兴趣小组对亚硝酸钠进行多角度探究:
i.亚硝酸钠的制备
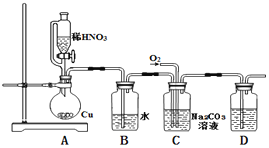
(1)实验中用恒压滴液漏斗,相比普通分液漏斗,显著的优点是____.
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为_______________。
ii. 探究亚硝酸钠与硫酸反应气体产物成分.
已知:①NO+NO2+2OH﹣═2NO2﹣+H2O ②气体液化的温度:NO2:21℃,NO:﹣152℃
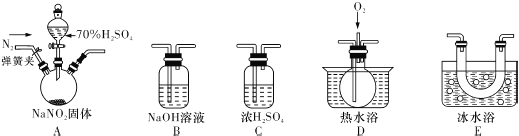
(3)反应前应打开弹簧夹,先通入一段时间氮气,目的是___________.
(4)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接):
A、C、______、______、______.
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体.
①确认A中产生的气体含有NO,依据的现象是_________________.
②装置B的作用是____________________.
iii. 设计实验证明酸性条件下NaNO2具有氧化性:___________。
供选用的试剂:NaNO2溶液、KMnO4溶液、FeSO4溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不合理的是

A. 装置①:证明元素非金属性强弱 S>C>Si
B. 装置②:四氯化碳萃取碘水中的碘
C. 装置③:制备并收集少量NO气体
D. 装置④:制备少量氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如下图,下列对该实验的描述错误的是( )

A. 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
B. 长玻璃管起冷凝回流作用
C. 不能用水浴加热
D. 加入过量乙酸可以提高1丁醇的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是
A. 苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯
B. 苯不能使酸性高锰酸钾褪色,说明苯环中没有碳碳双键
C. 甲烷中混有的乙烯可以用溴水除去
D. 医院用75%酒精杀菌、消毒,75%是指质量分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 氯化铁腐蚀铜板:Fe3++Cu===Fe2++Cu2+
B. 实验室制氯气:MnO2+4HCl(浓)![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
C. 稀硫酸中加氢氧化钡溶液至溶液呈中性:Ba2++H++OH-+SO![]() ===BaSO4↓+H2O
===BaSO4↓+H2O
D. 用氢氧化钠溶液吸收少量二氧化硫:2OH-+SO2 ===SO![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上的许多反应工艺来源于实验室里的简单操作,比如用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如下:
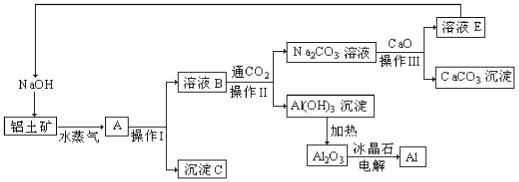
请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式_____________。
(2)沉淀C的颜色和一种用途分别为______________________________。
(3)操作I、操作II、操作III都用到的玻璃仪器是有_______________。
(4)整个生产过程中,除可以循环使用的物质有___________________(任意两种,填化学式)。用此法制取铝的副产品是________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com