
����Ŀ�������£���0.10mol/LNaOH��Һ�ζ�20.00mL 0.10mol/LHA��Һ(�ζ�����ͼ)������˵����ȷ����
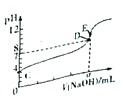
A. ��ͼ���Ա�ʾ��NaOH�ζ����������
B. ͼ��D��״̬ʱ��Һ���У�c(Na+)��c(A-)
C. �ﵽD��E״̬ʱ�����У�c(Na+)+c(H+)=c(A-)+c(OH-)
D. ��O<V(NaOH)<20.00mLʱ����Ӧ�����Һ�и�����Ũ���ɴ�С��˳���Ϊc(A-)> c(Na+)> c(H+)>c(OH-)
���𰸡�C
��������A������ͼ֪��HAδ������������ҺʱpH=3��HA��Ũ����0.1mol/L������HA�����ᣬ��������ǿ�ᣬ��A����B��ͼ��D����Һ�����ԣ����ݵ���غ�c(Na+)+c(H+)=c(A-)+c(OH-)����֪��ʱ��Һ��c(Na+)=c(A-)����B����C���ﵽD��E״̬ʱ����Һ�о����ڵ���غ�ʽc(Na+)+c(H+)=c(A-)+c(OH-)����C��ȷ��D����0mL��V��NaOH����20.00mLʱ�����������Һ�����ԣ�����c��H+����c��OH-��������������Ƶ������٣�����Һ��c��H+����c��Na+��������������Ƶ���ΪHA��һ�룬��c��Na+��=c��H+��������������Ƶ����϶�ʱ����c��Na+����c��H+������D����ΪC��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ��������ͼ��ʾ������Wԭ�ӵ���������������������������������˵������ȷ����
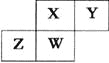
A. ԭ�Ӱ뾶:W>Z>Y>X
B. ����������Ӧˮ��������ԣ�X>W>Z
C. �����̬�⻯������ȶ���:Y>X>W>Z
D. Ԫ��X��Z��W������ϼ۷ֱ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������;�㷺��������ָʾ���ʹ����Ʊ���һ������ˮ�ܿ����Ҫ�ɷ�ΪCo2O3��������Fe2O3��Al2O3��MnO��MgO��CaO�ȣ���ȡCoC2O4��2H2O�����������£�

��֪��������Һ���е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Ca2+��Mg2+��Al3+�ȣ�
������������������������ʽ����ʱ��Һ��pH���±���
������ | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
��ȫ������pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��1�����������м���Na2SO3��Ŀ���ǽ�_____________��ԭ�������ӷ��ţ��Ա�����ܽ⡣�ò���Ӧ�����ӷ���ʽΪ ��дһ������
��2��NaClO3�������ǽ�����Һ�е�Fe2+������Fe3+����Ԫ�ر���ԭΪ��ͼۡ��÷�Ӧ�����ӷ���ʽΪ ��
��3������ƽ���ƶ�ԭ����������Na2CO3��ʹ����Һ��Fe3+��Al3+ת�����������������ԭ���� ��
��4����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ��ʾ����Һ���м�����ȡ���������� ��ʹ����ȡ�����˵�pH=____������ţ����ң�
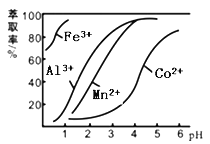
A��2.0 B��3.0 C�� 4.0
��5����Һ�����ơ�þ���ǽ���Һ��Ca2+��Mg2+ת��ΪMgF2��CaF2��������֪Ksp(MgF2)��7.35��10-11��Ksp(CaF2)��1.05��10-10�����������NaF��������Һc(Mg2+)/c(Ca2+)�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���һ���ͷų���������
A. ���л��Ϸ�Ӧ B. ���зֽⷴӦ C. ���Ӳ��ԭ�� D. ԭ����ɷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪HCN(aq)��NaOH(aq)��Ӧ����1 mol���ε���H����12.1 kJ/mol��ǿ�ᡢǿ���ϡ��Һ��Ӧ���к�����H����57.3 kJ��mol��1����HCN��ˮ��Һ����������H���ڣ� ��
A. ��69.4 kJ��mol��1 B. ��45.2 kJ��mol��1
C. ��69.4 kJ��mol��1 D. ��45.2 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ࡢ��֬����������������Ҫ��Ӫ�����ʣ������ǵķ���ʽ�� �������� �� �������ڵ��ǣ����ǵķ���ʽ�� ����������һ��������ˮ����������Ƿ��ӣ��������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CH4����ԭNOX�������������������Ⱦ��������
��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H1
��CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H2=-1160kJmol-1
��֪NO�� NO2���������ܶ�����ͬ�����������ܶȵ�17����16g����û������ǡ����ȫ��Ӧ����N2�� CO2��H2O(g)�ų�1042.8 kJ������������H1��( )
A��-574kJmol-1 B��-691.2kJmol-1 C��-867kJmol-1 D��-925.6kJmol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����ȡ����Ӧ����
A. ���������� B. ��ϩ���Ҵ� C. ������������� D. �Ҵ�����ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ơ���˼ά��һ����ʽ��������Ҳ�в��Եģ����С����ơ�����ȷ����
A��Fe��Cu���Ӳ���ϡ�������γɵ�ԭ��أ�FeΪ��������ôFe��Cu���Ӳ���Ũ������Һ���γɵ�ԭ��أ�FeҲΪ����
B��Cl2��H2O![]() HCl+HClO��������ԭ��Ӧ����ICl��H2O
HCl+HClO��������ԭ��Ӧ����ICl��H2O![]() HCl+HIOҲ��������ԭ��Ӧ
HCl+HIOҲ��������ԭ��Ӧ
C��þ�������ã���ҵ���õ���������������������Թ�ҵ��Ҳ�õ����������þ��þ
D����������Һͨ����������ɫ���Լ�ƿ�У�����Ϊ�����������ֽ�,��ôŨ������ҺҲҪ��������ɫ�Լ�ƿ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com