
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.分别在这两种物质的溶液中,加入少量澄清石灰水
B.分别加热这两种固体,将生成的气体通入澄清石灰水中
C.分别在这两种物质的溶液中,加入少量氯化钙溶液
D.分别在这两种物质的等浓度的溶液中,加入少量的稀盐酸
科目:高中化学 来源: 题型:
下列有关铁及其化合物的说法中不正确的是
A.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4
C.工业上可用铁质容器储存、运输浓硝酸和浓硫酸
D.氯化铁溶液有较强氧化性,故可用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示。下列描述正确的是( )
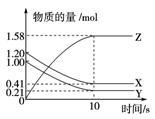
A、反应开始到10 s,用Z表示的反应速率为0.158 mol·(L·s)-1
B、反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1
C、反应开始到10 s时,Y的转化率为79.0 %
D、反应的化学方程式为:X(g)+Y(g)  Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
在200 mL氯化镁和氯化铝的混合液中,Mg2+的物质的量浓度为0.2 mol·L-1,Cl-的物质的量浓度为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需要加入4 mol·L-1 NaOH溶液的体积为
A.40 mL B.72 mL C.80 mL D.128 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中的两种物质作用,反应条件(温度或反应物用量)改变,不会引起产物种类改变的是
A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.AlCl3和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
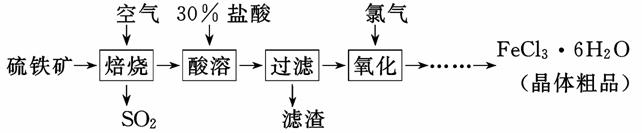
回答下列问题:
Ⅰ、(1)在一定条件下,SO2转化为SO3的化学反应为2SO2(g)+O2(g) 2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 。
2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是 、 。
(3)通氯气氧化时,发生的主要反应的离子方程式为 ;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为 (写化学式)。
Ⅱ、 已知: CuCl2溶液中含有少量杂质FeCl2,为制备纯净的CuCl2·2H2O晶体,拟定实验步骤如图所示:
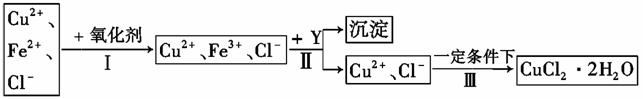
请回答下列问题:
(4)步骤Ⅰ中,将Fe2+转化为Fe3+最好选用下列氧化剂中的 (填字母)。
A.K2Cr2O7 B.NaClO C.H2O2
该反应的离子方程式为 。
(5)在步骤Ⅱ中,加入Y的目的是为了调节溶液的酸度以促使Fe3+沉淀完全,Y可以是下列物质中的 (填字母)。
A.NaOH B.Cu C.Cu2(OH)2CO3
(6)步骤Ⅲ应控制的实验条件是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
浓H2SO4 密度1.84g/mL,物质的量浓度为18.4 mol/L , 质量分数为98% ,取10mL浓H2SO4和amL水混合得物质的量浓度为Cmol/L,质量分数为b%。下列组合正确的是
(1). 若b=49 则a=18.4 C>9.2 (2) 若b=49 则a=18.4 C<9.2
(3). 若C=9.2 则a>10 b>49% (4) 若C=9.2 则a>10 b<49%
A.(1) (3) B.(1) (4) C.(2) (3) D.(2) (4)
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应精制CuO,其设计的实验过程为:
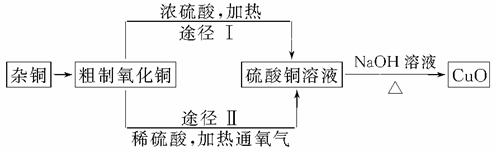
(1)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,灼烧后含有少量铜的可能原因是________。
a.灼烧过程中部分氧化铜被还原
b.灼烧不充分铜未被完全氧化
c. 氧化铜在加热过程中分解生成铜
氧化铜在加热过程中分解生成铜
d.该条件下铜无法被氧气氧化
(2)由粗制氧化铜通过两种途径制取纯净CuO,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是_______________________________________________________________________。
(3)有同学指出,由CuSO4溶液到生成CuO少了一个环节,即应先生成Cu(OH)2沉淀,过滤洗涤后再加热分解Cu(OH)2得CuO。以下说法不可能成为减少该环节的理由的是________。
A.CuO比Cu(OH)2颗粒粗大,更易于过滤从溶液中分离
B.Cu(OH)2 分解温度较低,加热其浊液即可使其分解
分解温度较低,加热其浊液即可使其分解
C.干态下分解Cu(OH)2,温度难以控制,可能因温度过高导致CuO进一步分解生成Cu2O
D.过滤分离出的CuO不需洗涤就已非常纯净
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com