
某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应精制CuO,其设计的实验过程为:
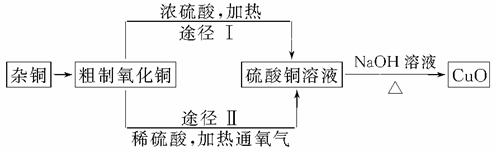
(1)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,灼烧后含有少量铜的可能原因是________。
a.灼烧过程中部分氧化铜被还原
b.灼烧不充分铜未被完全氧化
c. 氧化铜在加热过程中分解生成铜
氧化铜在加热过程中分解生成铜
d.该条件下铜无法被氧气氧化
(2)由粗制氧化铜通过两种途径制取纯净CuO,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是_______________________________________________________________________。
(3)有同学指出,由CuSO4溶液到生成CuO少了一个环节,即应先生成Cu(OH)2沉淀,过滤洗涤后再加热分解Cu(OH)2得CuO。以下说法不可能成为减少该环节的理由的是________。
A.CuO比Cu(OH)2颗粒粗大,更易于过滤从溶液中分离
B.Cu(OH)2 分解温度较低,加热其浊液即可使其分解
分解温度较低,加热其浊液即可使其分解
C.干态下分解Cu(OH)2,温度难以控制,可能因温度过高导致CuO进一步分解生成Cu2O
D.过滤分离出的CuO不需洗涤就已非常纯净
科目:高中化学 来源: 题型:
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.分别在这两种物质的溶液中,加入少量澄清石灰水
B.分别加热这两种固体,将生成的气体通入澄清石灰水中
C.分别在这两种物质的溶液中,加入少量氯化钙溶液
D.分别在这两种物质的等浓度的溶液中,加入少量的稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2(g)+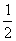 O2(g)====H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)====H2O(l) ΔH=-285.8 kJ·mol-1
CO(g)+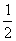 O2(g) ====CO2(g) ΔH=-283.0 kJ·mol-1
O2(g) ====CO2(g) ΔH=-283.0 kJ·mol-1
C8H18(l)+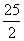 O2(g) ====8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
O2(g) ====8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
CH4(g)+2O2(g) ====CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是( )
A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
关于Al、Fe、Cu三种金属, 下列说法正确的是
下列说法正确的是
A.三者的单质均为银白色固体
B.三者都能与盐酸、稀硫酸反应
C.AlCl3、FeCl3、CuCl2均可作净水剂
D.制备Al用电解法,制备Fe、Cu可用还原法
查看答案和解析>>
科目:高中化学 来源: 题型:
美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示)。下列有关该工艺的说法错误的是
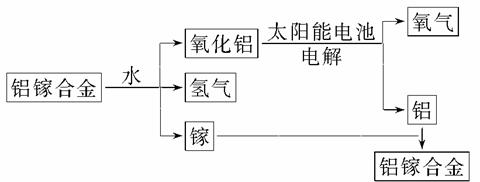
A.该过程中,能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金与水反应的化学方程式为:2Al+3H2O===Al2O3+3H2↑
D.总反应式为2H2O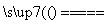 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
金刚砂(SiC)可由SiO2和碳在一定条件下反应制得,反应方程式为SiO2+3C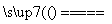 SiC+2CO↑,下列有关制造金刚砂的说法中正确的是
SiC+2CO↑,下列有关制造金刚砂的说法中正确的是
A.该反应中的氧化剂是SiO2,还原剂为C
B.该反应中的氧化产物 和还原产物的物质的量之比为1∶2
和还原产物的物质的量之比为1∶2
C.该反应中转移的电子数为12e-
D.该反应中的还原产物是SiC、氧化产物是CO,其物质的量之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.通常状况下,3.36升氯气与2.7克铝充分反应转移的电子数小于0.3NA
B.100g 98%的浓硫酸溶液中含氧原子个数为4NA C.1mol二氧化硅晶体中含有2NA个硅氧键
D.0.1L 3mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com