
| A.1.0mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
| C.pH=12的溶液:K+、Na+、CH3COO-、Br- |
| D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Cu2+、Cl-、SO42- | B.Fe3+、K+、SO42-、NO3- |
| C.H+、Al3+、OH-、NO3- | D.Na+、Ca2+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu2+、Fe3+、SCN-、K+ | B.Ba2+、AlO2-、OH-、Na+ |
| C.Cl-、H+、Na+、SO32- | D.ClO-、Na+、 Fe2+、 H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含有大量OH-的溶液:Na+、K+、NO3-、CO32- |
| B.含有大量H+的溶液:HCO3-、K+、SO42-、Cl- |
| C.含大量Fe3+的溶液:NH4+、Na+、SCN-、OH- |
| D.含有大量CO32-的溶液:Ca2+、Na+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4+、Ba2+、NO3—、CO32— | B.Cu2+、Fe3+、NO3-、SO42— |
| C.K+、Mg2+、Cl—、SO42— | D.Na+、K+、HCO3—、Cl— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
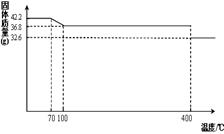
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+ 、K+、Cl-、 NO3- | B.Cu2+、K+、SO42-、NO3- |
| C.Na+、 K+、SO42-、HCO3- | D.Fe3+、K+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+) + c(NH4+)= c(Cl-)+ c(OH-) |
| B.c(Cl-)> c(NH4+)> c(OH-)> c(H+) |
| C.升高温度NH4+ 浓度变小 |
| D.加入少量NaOH溶液后,n(NH3·H2O)变小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com