
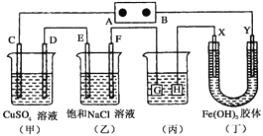
【题目】如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。则以下说法正确的是 ( )
A. 电源B极是正极
B. (甲)(乙)装置的C、D、E、F电极均有单质生成,其物质的量比为1:2:2:2
C. 欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D. 装置(丁)中Y极附近红褐色变浅,说明氢氧化铁胶粒带正电荷
【答案】B
【解析】乙装置为电解饱和食盐水,阴极反应为2H++2e-=H2↑,剩余水电离的氢氧根离子,溶液显碱性,所以F是电解的阴极,推出B为电源的负极,选项A错误。因为B为负极,A为正极,所以C、E、G、X为电解的阳极,D、F、H、Y为电解的阴极。C电极的反应为4OH- - 4e- = O2↑+ 2H2O,D电极的反应为Cu2+ + 2e- = Cu,E电极的反应为2Cl- -2e- = Cl2↑,F电极的反应为2H++2e-=H2↑,当各电极转移电子数相等时,都得到单质,且物质的量之比为1:2:2:2,选项B正确。电镀时应该选择镀层金属为阳极,所以铜上镀银,应该选择银为阳极,而图中H为电解的阴极,所以选项C错误。氢氧化铁胶粒带正电荷,在电解池中应该向阴极移动,Y为电解的阴极,所以是Y极附近颜色加深,选项D错误。


科目:高中化学 来源: 题型:
【题目】海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。
(1)工业上进行海水淡化有多种方法。
①蒸馏法是历史最久,技术和工艺比较成熟的海水淡化方法。下图是海水蒸馏装置示意图,仪器B的名称是_________。

②下图是膜分离技术进行海水淡化的原理示意图。水分子可以透过淡化膜,而海水中其他各种离子不能通过淡化膜。加压后,右侧海水中减少的是_______(填序号)。

a. 溶质质量 b. 溶液质量 c. 溶剂质量 d. 溶质的物质的量浓度
(2)碘在海水中主要以I-的形式存在,而在地壳中主要以IO3-的形式存在(几种粒子之间的转化关系如下图)。

①海水为原料按方法i制取I2的离子方程式是___________________。已知I2可以与Cl2继续反应生成IO3-,由该法制取I2时应注意控制的反应条件是_______。
②以方法ii在溶液中制取I2,反应的离子方程式是(已知:反应后所得溶液显酸性)________。
③上图iii中反应后溶液中IO3-和Cl-的个数比为1:6,则该反应中氧化剂和还原剂的物质的量之比是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(共6分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g)![]() Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
(1)该反应的氧化剂是 ,2molN2参加反应转移电子数为 。
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图。

图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中CO的含量最高的一段时间是 。
(3)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是
(提示:272 = 729)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关键角与分子空间构型的说法不正确的是( )
A. 键角为180°的分子,空间构型是直线形
B. 键角为120°的分子,空间构型是平面三角形
C. 键角为109.5°的分子,空间构型是正四面体形
D. 键角为90°~109.5°之间的分子,空间构型可能是V形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实对应的离子方程式不正确的是
A. 用碳酸钠溶液处理锅炉中的硫酸钙水垢:CaSO4(s)+ ![]() (aq)
(aq) ![]() CaCO3(s)+
CaCO3(s)+ ![]() (aq)
(aq)
B. 用加热的方法降低自来水中钙离子浓度:Ca2++2H![]()
![]() CaCO3 ↓+H2O+CO2↑
CaCO3 ↓+H2O+CO2↑
C. 用醋酸清洗热水壶中的碳酸钙水垢:2H++CaCO3=== Ca2++H2O+CO2↑
D. 用肥皂(主要成分C17H35COONa)检验含有较多钙离子的硬水:2C17H35COO—+Ca2+ === (C17H35COO)2Ca↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时下述反应的有关数据:C(s)+ ![]() O2(g)=CO(g)△H1=-110.5kJmol-1,C(s)+O2(g)=CO2(g)△H2=-393.5kJmol-1。则C(s)+CO2(g)=2CO(g)的△H为( )
O2(g)=CO(g)△H1=-110.5kJmol-1,C(s)+O2(g)=CO2(g)△H2=-393.5kJmol-1。则C(s)+CO2(g)=2CO(g)的△H为( )
A. +283.0kJ/mol B. +172.5 kJ/mol C. -172.5 kJ/mol D. -504 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为2H2+O2==2H2O,下列有关说法正确的是()

A. 电子通过外电路从b极流向a极
B. b极上的电极反应式为:O2+2H2O+4e-=4OH-
C. 每转移0.1 mol电子,便消耗1.12 升的H2
D. H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g)![]() 4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )
4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )
A. 前2 min,D的平均反应速率为0.2 mol/(L·min)
B. 此时,B的平衡转化率是40%
C. 增大该体系的压强,平衡不移动
D. 增加B,平衡向右移动,B的平衡转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com