
【题目】将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解(产生气体全部逸出),冷却后将溶液稀释至1000ml,测得c(H+)=0.84mol/L;若要使稀释后溶液中的Cu2+沉淀完全,应加入6.0mol/L的NaOH溶液的体积为:
A.100mLB.160mLC.240mLD.307mL
【答案】D
【解析】
反应剩余硫酸的物质的量为:![]() ×0.84mol/L×1L=0.42mol,设混合物中含铜、氧化铜的物质的量分别为x、y,则:
×0.84mol/L×1L=0.42mol,设混合物中含铜、氧化铜的物质的量分别为x、y,则:
Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
1 2 1
x 2x x
CuO+H2SO4═CuSO4+H2O
1 1
yy
所以,2x+y=18.4mol/L×0.05L-0.42mol=0.5mol,64g/molx+80g/moly=20.8g,解得:x=0.2mol,y=0.1mol,n(SO2)=0.2mol,1000mL溶液中SO42-的总量为18.4mol/L×0.05L-0.2mol=0.72mol,Cu2+刚好沉淀完全,此时溶液中溶质为Na2SO4,根据钠离子守恒n(NaOH)=2n(Na2SO4),故需要n(NaOH)=2n(Na2SO4)=0.72mol×2=1.44mol,所以沉淀Cu2+所需氢氧化钠的体积=![]() =0.24L=240mL,故选C。
=0.24L=240mL,故选C。


科目:高中化学 来源: 题型:
【题目】 对此聚合物分析正确的是( )
对此聚合物分析正确的是( )
A. 其单体是CH2=CH2和HCOOC2H5
B. 它是缩聚反应产物
C. 其单体是CH2=CH-COOC2H5
D. 其链节是CH3CH2-COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将agFe2O3和Al2O3的样品溶解在过量的200mL物质的量浓度为0.05mol/L的H2SO4溶液中,然后向其中加入NaOH溶液使Al3+、Fe3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
A.0.1mol/LB.0.2mol/LC.0.4mol/LD.0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热测定实验中,下列说法错误的是
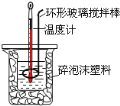
A.一组完整实验数据需要测温度三次
B.可用金属做的环形搅拌棒代替玻璃搅拌棒
C.烧杯间填满碎泡沫塑料是为了减少实验过程中热量散失
D.用0.5molL-1NaOH溶液分别与0.5molL-1的盐酸、硝酸溶液反应,如果所取的溶液体积相等,则测得的中和热数值相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2和NOx是主要大气污染物,利用下图装置可同时吸收SO2和NO。下列有关说法错误的是
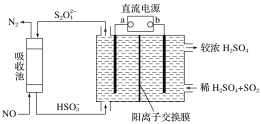
A.a极为直流电源的负极
B.阳极发生的反应式为SO2-2e-+2H2O=SO42-+4H+
C.阴极得到1mol电子时,通过阳离子交换膜的H+为2mol
D.吸收池中发生反应的离子方程式为:2NO+2S2O42-+2H2O=N2+4HSO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液![]() ,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解
,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解![]() 。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示
。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示![]() 已知硝酸只被还原为NO气体
已知硝酸只被还原为NO气体![]() 。下列分析或结果错误的是
。下列分析或结果错误的是

A.原混合酸中![]() 的物质的量为
的物质的量为![]()
B.OA段产生的是NO,AB段发生的反应为![]() ,BC段产生氢气
,BC段产生氢气
C.第二份溶液中最终溶质为![]()
D.![]() 浓度为
浓度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一](1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是_____________________。
(2)称取碳素钢6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______(选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液C.浓氨水 D.酸性KMnO4溶液
②乙同学取560 mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66 g。由此推知气体Y中SO2的体积分数为_______。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893 g·L-1。为此设计了下列探究实验装置(假设有关气体完全反应)。
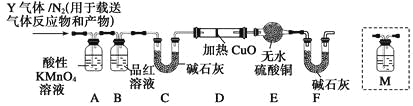
(3)装置B中试剂的作用是_______________________。
(4)分析Y气体中的Q2气体是如何生成的_____________(用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加洗气瓶M于_______(填序号)。
A.A之前 B.A—B间
C.B—C间 D.C—D间
(6)如果气体Y中含有Q1,预计实验现象应是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年,我国科学家研发出一种新型的锌碘单液流电池,已知M为阴离子交换膜,其原理如图所示。下列说法不正确的是
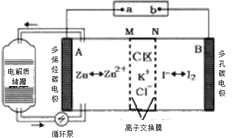
A.放电时A电极反应式为:Zn-2e﹣= Zn2+
B.充电时,B极与外接电源正极相连
C.放电时电解质储罐中离子浓度增大
D.放电时当A极减少65g时,C区Cl﹣增加2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com