

分析 根据流程图知,一定条件下,一氧化碳和氢氧化钠反应生成甲酸钠,反应方程式为:CO+NaOH$\frac{\underline{\;催化剂\;}}{\;}$HCOONa,加热条件下,甲酸钠脱氢生成草酸钠,由原子守恒可知有氢气生成,反应方程式为:2HCOONa$\frac{\underline{\;催化剂\;}}{\;}$Na2C2O4+H2↑.Na2C2O4与Ca(OH)2 反应得到CaC2O4和NaOH,过滤得滤渣CaC2O4,加入H2SO4,H2SO4与CaC2O4反应生成CaSO4和H2C2O4.
(1)加热条件下,甲酸钠脱氢生成Na2C2O4和H2;
(2)根据题意Na2C2O4与Ca(OH)2 反应得到CaC2O4和NaOH,过滤得滤渣CaC2O4,加入H2SO4,H2SO4与CaC2O4反应生成CaSO4和H2C2O4;
(3)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法;
(4)草酸晶体中含有结晶水;
(5)用烧杯溶解固体,酸性高锰酸钾置于酸式滴定管中,根据5H2C2O4+2MnO4-+6H+=1OCO2↑+2Mn2++8H2O计算;
(6)反应生成Mn2+.
解答 解:根据流程图知,一定条件下,一氧化碳和氢氧化钠反应生成甲酸钠,反应方程式为:CO+NaOH$\frac{\underline{\;催化剂\;}}{\;}$HCOONa,加热条件下,甲酸钠脱氢生成草酸钠,由原子守恒可知有氢气生成,反应方程式为:2HCOONa$\frac{\underline{\;催化剂\;}}{\;}$Na2C2O4+H2↑.Na2C2O4与Ca(OH)2 反应得到CaC2O4和NaOH,过滤得滤渣CaC2O4,加入H2SO4,H2SO4与CaC2O4反应生成CaSO4和H2C2O4.
(1)加热条件下,甲酸钠脱氢生成Na2C2O4和H2,方程式为:2HCOONa$\stackrel{△}{→}$Na2C2O4+H2↑,故答案为:2HCOONa$\stackrel{△}{→}$Na2C2O4+H2↑;
(2)Na2C2O4与Ca(OH)2 反应得到CaC2O4和NaOH,过滤得滤渣CaC2O4,加入H2SO4,H2SO4与CaC2O4反应生成CaSO4和H2C2O4,过滤得滤渣CaSO4,滤液H2C2O4溶液;
故答案为:Ca(OH)2;H2SO4;
(3)溶液得到草酸晶体,需要经蒸发浓缩、冷却结晶、过滤洗涤、干燥,故答案为:冷却结晶;过滤洗涤;
(4)草酸晶体中含有结晶水,不能证明有水生成,故答案为:H2O;草酸晶体中含有水;
(5)用烧杯溶解固体,酸性高锰酸钾置于酸式滴定管中,
由关系式 2KMnO4~5H2C2O4可知
2 5
0.04mol•L-1×0.025L n
n=0.001mol
草酸晶体的质量分数=$\frac{0.001mol×126g/mol}{0.250g}$×100%=50.4%,故答案为:烧杯;酸式滴定管;50.4%;
(6)生成的Mn2+对此反应起催化剂的作用,速率加快,随反应物浓度减小,反应速率减小,
故答案为:Mn2+;生成的Mn2+对此反应起催化剂的作用.
点评 主要考查了草酸的性质与制备,涉及知识点较多,综合性较强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | CO2和N2 | B. | CO2和NO2 | C. | CO2和O2 | D. | CO2、N2和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将固体CuO加入稀H2SO4中 CuO+2H+=Cu2++H2O | |
| B. | 盐酸滴加在石灰石上 CaCO3+2H+=Ca2++H2CO3 | |
| C. | Ba(OH)2溶液与稀硫酸混合 Ba2++SO42-=BaSO4↓ | |
| D. | 铜片加入稀盐酸中 Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
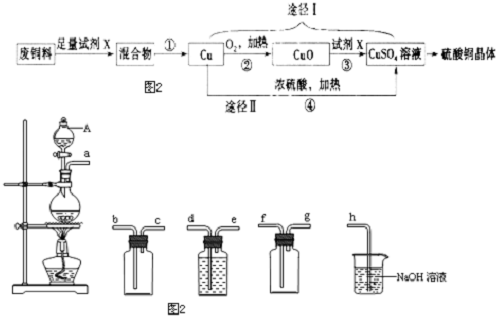
 氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:
氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
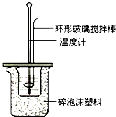 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  | 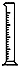 |
| 序号 | a | b | c | d | e | f |
 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 茉莉酮是一种人工合成的香料,其结构简式如图所示:
茉莉酮是一种人工合成的香料,其结构简式如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | |
| B. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 | |
| C. | “低碳生活”倡导生活中尽量减少耗能,从而减少CO2排放 | |
| D. | 铝表面有一层致密的氧化物薄膜,故铝制容器可用来腌制咸菜等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com