
 氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:
氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:分析 (1)根据仪器的构造可判断装置甲中仪器A的名称;该反应需要催化剂,则甲中活性炭的作用是催化剂;硫酰氯在潮湿空气中“发烟”,而空气中含有水蒸气;
(2)装置丁是提供氯气的,在酸性溶液中漂白粉能氧化氯离子生成氯气;
(3)氯磺酸(C1SO3H)加热分解,也能制得硫酰氯与另外一种物质,根据原子守恒可知另一种生成物是硫酸;硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,而硫酸沸点高;
(4)生成的氯气中含有氯化氢;氯气和二氧化硫可能发生反应生成硫酸;
(5)由于硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.
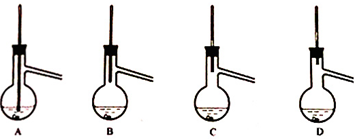
解答 解:(1)根据仪器的构造可判断装置甲中仪器A的名称为冷凝管或蛇形冷凝管或环形冷凝管;该反应需要催化剂,则甲中活性炭的作用是催化剂;硫酰氯在潮湿空气中“发烟”,而空气中含有水蒸气,则B的作用为防止水蒸气进入,故答案为:冷凝管或蛇形冷凝管或环形冷凝管;催化剂;防止水蒸气进入;
(2)装置丁是提供氯气的,在酸性溶液中漂白粉能氧化氯离子生成氯气,则装置丁中发生反应的离子方程式为Cl-+ClO-+2H+=Cl2↑+H2O,故答案为:Cl-+ClO-+2H+=Cl2↑+H2O;
(3)氯磺酸(C1SO3H)加热分解,也能制得硫酰氯与另外一种物质,根据原子守恒可知另一种生成物是硫酸,因此该反应的化学方程式为2C1SO3H$\frac{\underline{\;\;△\;\;}}{\;}$SO2Cl2+H2SO4;硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,而硫酸沸点高,则分离产物的方法是蒸馏,答案选C,故答案为:2C1SO3H$\frac{\underline{\;\;△\;\;}}{\;}$SO2Cl2+H2SO4;C;
(4)生成的氯气中含有氯化氢,所以装置丙的作用为除去HCl气体.氯气具有强氧化性,能氧化SO2,装置乙是干燥氯气的,因此若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为Cl2+SO2+2H2O=2HCl+H2SO4,故答案为:除去HCl气体;Cl2+SO2+2H2O=2HCl+H2SO4;
(5)由于硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解,因此为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有①先通冷凝水,再通气,②控制气流速率,宜慢不宜快,③若三颈烧瓶发烫,可适当降温,但不能加热三颈烧瓶,否则会加速分解,答案选①②③.故答案为:①②③.
点评 本题考查实验制备方案,涉及对反应原理、装置及操作的分析评价、对仪器的识别、物质的分离提纯等,注意对物质性质信息的应用,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ②④ | C. | ①③⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)减小,c(H+)减小 | |
| B. | 将水加热,KW增大,pH变小 | |
| C. | 向水中加入少量HCl气体,平衡逆向移动,c(H+)减小,c(OH-)减小 | |
| D. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3硬度高,熔点2054℃,沸点2980℃,属于原子晶体 | |
| B. | 在晶体中,只要有阴离子一定有阳离子 | |
| C. | 某固态单质能导电,该单质一定属于金属晶体 | |
| D. | SiO2分子中每个Si原子周围有4个O原子,每个O原子周围有2个Si原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义.
氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com