
| A. | Al2O3硬度高,熔点2054℃,沸点2980℃,属于原子晶体 | |
| B. | 在晶体中,只要有阴离子一定有阳离子 | |
| C. | 某固态单质能导电,该单质一定属于金属晶体 | |
| D. | SiO2分子中每个Si原子周围有4个O原子,每个O原子周围有2个Si原子 |
分析 A.离子化合物的构成微粒为离子,其熔融状态下能导电,而原子晶体不能,Al2O3属于离子晶体;
B.晶体中只要有阴离子,必定是离子晶体,所以一定有阳离子;
C.有些非金属单质为半导体,能导电;
D.每个Si原子周围有4个O原子;每个O原子与2个Si原子相连,但SiO2为原子晶体无分子.
解答 解:A.Al2O3硬度高,熔点2054℃,沸点2980℃,Al2O3熔融时能导电属离子晶体,故A错误;
B.在晶体中有阴离子,根据物质呈电中性,有阴离子,那么一定有阳离子中和阴离子的电性,故B正确;
C.硅是良好的半导体材料,单质硅是非金属单质,故C错误;
D.二氧化硅晶体中存在四面体结构单元,每个硅原子能构成四个共价键,每个氧原子能形成2个共价键,与2个Si原子相连,Si处于中心,O处于4个顶角,每个Si原子周围有4个O原子,为原子晶体无分子,故D错误;
故选B.
点评 本题考查了晶体的构成微粒、晶体类型,可根据物质的构成微粒判断晶体类型,但不能根据物质的熔点判断晶体类型,要注意的是:含阳离子的物质中不一定含阴离子,如金属晶体;但含阴离子的晶体一定含阳离子,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH3CH2Cl$→_{△}^{NaOH溶液}$CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2═CH2$\stackrel{Cl_{2}}{→}$CH2ClCH2Cl | |
| B. | CH3CH2Cl$\stackrel{Cl_{2}}{→}$CH2ClCH2Cl | |
| C. | CH3CH2Cl$→_{△}^{NaOH的醇溶液}$CH2═CH2$\stackrel{HCl}{→}$CH3CH2Cl$\stackrel{Cl_{2}}{→}$CH2ClCH2Cl | |
| D. | CH3CH2Cl$→_{△}^{NaOH的醇溶液}$CH2═CH2$\stackrel{Cl_{2}}{→}$CH2ClCH2Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将固体CuO加入稀H2SO4中 CuO+2H+=Cu2++H2O | |
| B. | 盐酸滴加在石灰石上 CaCO3+2H+=Ca2++H2CO3 | |
| C. | Ba(OH)2溶液与稀硫酸混合 Ba2++SO42-=BaSO4↓ | |
| D. | 铜片加入稀盐酸中 Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:
氯化法是合成硫酰氯(SO2Cl2)的常用方法,实验室合成硫酰氯(SO2Cl2)的反应和实验装置如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
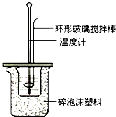 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol N2(g)和3 mol H2(g)的能量之和高于2 mol NH3 (g)的能量 | |
| B. | 形成2 mol NH3(g)的化学键释放的总能量大于断裂1 mol N2 (g) 和3 mol H2 (g) 的化学键所吸收的总能量 | |
| C. | 加入催化剂是为了加大反应速率,缩短生产周期,降低生产成本 | |
| D. | 将1 mol N2(g)和3 mol H2(g)充入一密闭容器中充分反应,放出92.2 kJ 的热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com