
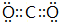 ,故答案为:
,故答案为: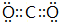 ;
; ,用电子式表示其形成过程为:
,用电子式表示其形成过程为: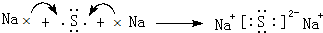 ,
,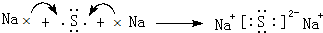 .
.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
| A、一定形成共价键 |
| B、一定形成离子键 |
| C、可能形成共价键,也可能形成离子键 |
| D、以上说法都不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
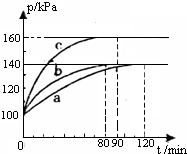 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程如下.
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程如下.查看答案和解析>>
科目:高中化学 来源: 题型:
 煤是重要的能,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
| ||
| O2/H2O |
| n(O2) |
| n(NH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定有乙烯 |
| B、一定有甲烷 |
| C、一定没有甲烷 |
| D、一定没有乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在中和热测定实验中,为准确测得反应前后的温差,应将已分别测得温度的氢氧化钠溶液与盐酸在隔热的容器中快速混合,并不断搅拌,用温度计测量混合液的最高温度 |
| B、往海带灰的浸泡液中加入过量的氯水,保证I-完全氧化为I2 |
| C、将溴乙烷与氢氧化钾混合液加热,再滴加硝酸银溶液,观察有淡黄色沉淀生成,可证明溴乙烷中含有溴 |
| D、润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
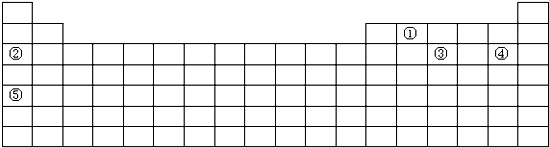
| 周期数 | 一 | 二 | 三 | 四 | 五 | 六 | 七 |
| 元素种数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述I | 陈述II |
| A | SO2有漂白性 | SO2能使紫色石蕊试液褪色 |
| B | 浓硫酸具有吸水性 | 蓝色硫酸铜晶体加入到浓硫酸中变白色 |
| C | 在一定条件下铁与水可以发生反应 | 将水蒸气通过灼热的铁粉,粉末变红 |
| D | 有些反应是吸热反应 | 这些反应一定是在高温条件下发生 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com